题目内容
13.下列微粒只有氧化性的是( )| A. | H+ | B. | Fe2+ | C. | Br - | D. | Cl2 |
分析 根据化合价的高低判断微粒的氧化性还原性,最高价态的只有氧化性,最低价态的只有还原性,中间价态的既有氧化性又有还原性,以此解答该题.
解答 解:A.H+的化合价是最高价,所以只有氧化性,故A正确;
B.Fe的化合价有0、+2、+3价,Fe2+处于中间价态,既具有氧化性也具有还原性,故B错误;
C.Br元素化合价为最低价态,只具有还原性,故C错误;
D.Cl2中Cl的化合价是中间价态,所以既有氧化性又有还原性,故D错误.
故选A.
点评 本题考查氧化还原反应及微粒的性质,为高频考点,明确氧化性、还原性与微粒中元素的化合价的关系是解答本题的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.设NA为阿伏伽德罗常数的值,下列叙述不正确的是( )
| A. | 含16g氧原子的二氧化硅晶体中含有的δ键数目为2NA | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 12克石墨中含有的共价键数目为1.5NA | |
| D. | 2molSO2和1molO2在一定条件下反应所得混合气体分子数等于2 NA |
4.化学与生活、社会发展息息相关,下列说法正确的是( )
| A. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| B. | 用乙醚从黄花蒿中提取青蒿素是利用了氧化还原反应原理 | |
| C. | “丹砂(HgS)烧之成水银,积变又成丹砂.”这个过程是可逆反应 | |
| D. | 丁达尔效应可用于区别溶液与胶体,云、雾、稀硫酸均能产生丁达尔效应 |
1.下列说法错误的是( )
| A. | 甲烷分子是正四面体结构 | B. | 丙炔分子中的碳原子在同一直线上 | ||
| C. | 有机分子中碳原子均形成四个价键 | D. | 二氟甲烷的有2种同分异构体 |
18.常温下,下列反应产生氢气最多的是( )
| A. | 1.12 g铁与足量浓硫酸反应 | |
| B. | 0.12g镁与足量盐酸反应 | |
| C. | 0.02mol钠与足量水反应 | |
| D. | 0.01mol铝与足量氢氧化钠溶液反应 |
5.下列反应的离子方程式正确的是( )
| A. | 实验室用大理石和稀盐酸制取二氧化碳:2H++CO32-→CO2↑+H2O | |
| B. | 铁片溶于稀硫酸中:2Fe+6H+→2Fe3++3H2↑ | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-→Al(OH)3↓ | |
| D. | 氢氧化铜溶于稀盐酸中:Cu(OH)2+2H+→2H2O+Cu2+ |
2.已知常温下0.1mol•L-1NH4HCO3溶液的pH=7.8,溶液中含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )


| A. | 常温下,碳酸的第一、二步电离常数之比为K1:K2=102.9 | |
| B. | NH4HCO3溶液中:c(HCO3-)>c(NH4+)>c(OH-)>c(H+) | |
| C. | NH4HCO3溶液中:c(NH4+)+c(NH3•H2O)+c(H+)=c(CO32-)+c(H2CO3)+c(HCO3-)+c(OH-) | |
| D. | 常温下,NH3•H2O的电离常数大于H2CO3的第一步电离常数 |
1.将一铁、铜混合物粉末平均分成三等份,分别加入到同浓度、不同体积的稀硝酸中,充分反应后,收集到NO气体的体积及剩余固体的质量如表 (设反应前后溶液的体积不变,气体体积已换算为标准状况时的体积):
下列说法正确的是( )
| 实验序号号 | 稀硝酸的体积/mL | 剩余固体的质量/g | NO的体积/L |
| 1 | 100 | 17.2 | 2.24 |
| 2 | 200 | 8.00 | 4.48 |
| 3 | 400 | 0 | V |
| A. | 表中 V=7.84 L | |
| B. | 原混合物粉末的质量为25.6 g | |
| C. | 原混合物粉未中铁和铜的物质的量之比为2:3 | |
| D. | 实验3所得溶液中硝酸的物质的量浓度为0.875 mol•L-1 |

 .
.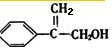 .写出反应⑥的化学方程式(注明必要的反应条件):
.写出反应⑥的化学方程式(注明必要的反应条件): +CH3OH$→_{△}^{浓H_{2}SO_{4}}$
+CH3OH$→_{△}^{浓H_{2}SO_{4}}$ .
.