题目内容
19.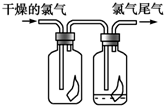 (1)如图所示,将氯气依次通过盛有干燥的有色布条和湿润的有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.
(1)如图所示,将氯气依次通过盛有干燥的有色布条和湿润的有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.(2)为防止氯气污染空气,可用NaOH溶液吸收多余的氯气,原理是Cl2+2NaOH=NaCl+NaClO+H2O(用化学方程式表示).根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是Ca(ClO)2(填化学式,下同),长期露置于空气中的漂白粉,加入稀盐酸后产生的气体是CO2.
(3)氯气泄漏时,人们需尽快远离现场,可用浸有一定浓度某物质水溶液的毛巾捂住口鼻,最适宜采用的物质是D.
A.NaOH B.NaCl C.KBr D.Na2CO3.
分析 (1)氯气无漂白性,氯气与水反应生成的次氯酸具有漂白性;
(2)利用氯气和氢氧化钠溶液反应来处理尾气;石灰乳吸收工业氯气尾气制得漂白粉生成氯化钙、次氯酸钙,长期露置于空气中的漂白粉,变质生成碳酸钙,加稀盐酸后产生的气体为二氧化碳;
(3)强碱具有腐蚀性,利用弱碱性溶液吸收氯气.
解答 解:(1)氯气无漂白性,氯气与水反应生成的次氯酸具有漂白性;Cl2+H2O=HCl+HClO;干燥的有色布条无明显现象,潮湿的有色布条褪色,
故答案为:干燥的有色布条无明显现象,潮湿的有色布条褪色;
(2)为了防止氯气尾气污染空气,可用NaOH溶液吸收,该反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O,离子反应为Cl2+2OH-=Cl-+ClO-+H2O,漂白粉的有效成分是次Ca(ClO)2;长期露置于空气中的漂白粉,会和空气中的二氧化碳水反应生成碳酸钙和次氯酸,次氯酸分解,最后主要含碳酸钙,加稀盐酸后产生的气体是二氧化碳,
故答案为:NaOH;Cl2+2NaOH=NaCl+NaClO+H2O;Ca(ClO)2;CO2;
(3)当氯气泄漏人们逃离现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,水溶液能较易吸收氯气,但不能对人有腐蚀作用;
A.NaOH是强碱具有强腐蚀性,故不选;
B.NaCl不能吸收氯气,故不选;
C.KBr反应生成溴蒸气,故不选;
D.Na2CO3溶液水解显碱性,可以吸收氯气,腐蚀性较小,符合要求,故选;
故答案为:D.
点评 本题考查氯气的性质及实验装置,为高频考点,把握氯气与水、碱的反应及尾气处理等为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列离子方程式不正确的是( )
| A. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓ | |
| B. | 氨水中通入过量SO2:NH3•H2O+SO2═HSO3-+NH4+ | |
| C. | 饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O |
14.运用有关概念判断下列说法中不正确的是( )
①BaSO4的水溶液不易导电,故BaSO4是弱电解质
②同位素的性质几乎完全相同
③利用Br2与I2分别与足量的H2反应的难易,判断溴与碘的非金属活动性强弱
④电子数相同的粒子不一定是同一种元素
⑤一种元素只能有一种质量数
⑥互称同位素的两种核素间具有相同的中子数和核外电子数.
①BaSO4的水溶液不易导电,故BaSO4是弱电解质
②同位素的性质几乎完全相同
③利用Br2与I2分别与足量的H2反应的难易,判断溴与碘的非金属活动性强弱
④电子数相同的粒子不一定是同一种元素
⑤一种元素只能有一种质量数
⑥互称同位素的两种核素间具有相同的中子数和核外电子数.
| A. | ①②④⑤ | B. | ③④⑤⑥ | C. | ②③⑤⑥ | D. | ①②⑤⑥ |
3.工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)?Si(s)+4HCl(g)△H=+Q kJ•mol-1(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是( )
| A. | 反应过程中,若增大压强能提高SiCl4的转化率 | |
| B. | 若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ | |
| C. | 反应至4 min时,若HCl浓度为0.12 mol•L-1,则H2的反应速率为0.03 mol•(L•min-1) | |
| D. | 当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol•L-1的NaOH溶液中恰好反应 |
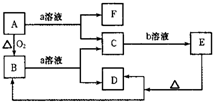 已知如图中A是固体单质,E是一种白色沉淀,F为密度最小的无色气体.且各种物质所含元素除H、O外,其余均为第三周期元素.
已知如图中A是固体单质,E是一种白色沉淀,F为密度最小的无色气体.且各种物质所含元素除H、O外,其余均为第三周期元素.