题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、0.1mol?L-1 Na2S溶液中含有的Na+离子数为0.2NA |
| B、50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| C、标准状况下,22.4L以任意比例混合的氢气和氯气混合气中含有的原子总数为2NA |
| D、0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、溶液中硫离子使弱酸阴离子水解减小;
B、浓硫酸随反应进行,浓度减小为稀硫酸不与铜发生反应;
C、依据n=
计算物质的量,结合氢气和氯气都是双原子分子分析;
D、依据化学方程式定量关系计算分析.
B、浓硫酸随反应进行,浓度减小为稀硫酸不与铜发生反应;
C、依据n=
| V |
| 22.4 |
D、依据化学方程式定量关系计算分析.
解答:
解:A、溶液中硫离子使弱酸阴离子水解减小,0.1mol?L-1 Na2S溶液中含有的Na+离子数小于0.2NA,故A错误;
B、浓硫酸随反应进行,浓度减小为稀硫酸不与铜发生反应,生成SO2分子数目小于0.46NA,故B错误;
C、依据n=
计算物质的量=
=1mol,结合氢气和氯气都是双原子分子,22.4L以任意比例混合的氢气和氯气混合气中含有的原子总数为2NA,故C正确;
D、依据化学方程式定量关系计算,3Fe+4H2O=Fe3O4+4H2,0.10mol Fe粉与足量水蒸气反应生成的H2分子数为
NA,故D错误;
故选C.
B、浓硫酸随反应进行,浓度减小为稀硫酸不与铜发生反应,生成SO2分子数目小于0.46NA,故B错误;
C、依据n=
| V |
| 22.4 |
| 22.4L |
| 22.4L/mol |
D、依据化学方程式定量关系计算,3Fe+4H2O=Fe3O4+4H2,0.10mol Fe粉与足量水蒸气反应生成的H2分子数为
| 0.4 |
| 3 |
故选C.
点评:本题考查了阿伏伽德罗常数的分析判断,主要是溶液中盐类水解分析,气体摩尔体积的条件应用,注意浓硫酸变稀后不与铜发生反应,题目难度中等.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
下列离子或分子组能大量共存,且满足相应要求的是( )
| A、Na+、K+、Ag+、NO3- 要求:逐滴滴加氨水先有沉淀产生,后沉淀消失 |
| B、Fe3+、NO3-、I-、HCO3- 要求:逐滴滴加盐酸立即有气体产生 |
| C、K+、AlO2-、Cl-、MnO4- 要求:无色澄清溶液 |
| D、NH4+、Al3+、SO42-、CH3COOH 要求:逐滴滴加NaOH溶液立刻有气体产生 |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、30g SiO2含有NA个Si-O共价键 |
| B、1L 0.2mol?L-1 Al2(SO4)3溶液中的离子总数为NA |
| C、标准状况下,22.4L H2O所含原子个数大于3NA |
| D、含4mol HCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数为NA |
下列实验操作或装置符合实验要求的是( )


| A、装置Ⅰ可用于测定中和热 |
| B、装置Ⅱ装置放置一段时间后,饱和CuSO4溶液中不出现蓝色晶体 |
| C、装置Ⅲ中的石英坩埚可用于熔化氢氧化钠 |
| D、装置Ⅳ可用于吸收易溶于水的尾气 |
下列实验装置能达到实验目的是( )
A、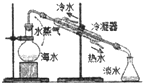 海水蒸馏 |
B、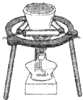 钾在空气中的燃烧 |
C、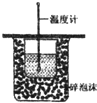 测定中和热 |
D、 牺牲阳极的阴极保护法 |
某有机物M的结构简式如图所示,下列有关叙述正确的是( )


| A、1mol M最多可以与2mol Br2发生反应 |
| B、M在一定条件下可以发生消去反应、取代反应和加成反应 |
| C、一个M分子中最多有8个碳原子在同一平面上 |
| D、1mol M与足量的NaOH溶液反应,最多可以消耗3mol NaOH |
 试运用所学知识,解决下列问题:
试运用所学知识,解决下列问题: