题目内容
9.将纯锌片和纯铜片按下图插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )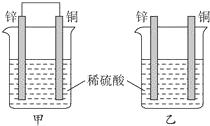
| A. | 两烧杯中溶液的pH值均增大 | B. | 产生气泡的速率甲比乙快 | ||
| C. | 两烧杯中铜片表面均无气泡产生 | D. | 甲中铜片是正极,乙中锌片是负极 |
分析 甲中形成铜锌原电池,锌作负极,失电子,铜作正极,H+在铜极上得电子,生成H2,总反应式为:Zn+H2SO4=ZnSO4+H2↑.乙装置中只是锌片与稀硫酸间发生了置换反应:Zn+H2SO4=ZnSO4+H2↑,以此进行分析.
解答 解:A.甲中铜片上氢离子得电子生成氢气,乙中锌和稀硫酸发生置换反应生成氢气,所以两烧杯的溶液中氢离子浓度均减小,溶液的pH值都增大,故A正确;
B.甲能形成原电池,乙不能构成原电池,所以产生气泡的速度甲比乙快,故B正确;
C.甲中形成铜锌原电池,锌作负极,失电子,铜作正极,H+在铜极上得电子,生成H2,所以甲中铜片表面有气泡产生,故C错误;
D.乙中不构成原电池,锌片不是电极,故D错误;
故选AB.
点评 本题考查了置换反应和原电池的有关知识,题目难度不大,注意把握原电池的组成条件的工作原理.

练习册系列答案
相关题目
19.下列化学用语的使用正确的是( )
| A. | 氯化铵的电子式为  | |
| B. | 重氢负离子(${\;}_{1}^{2}$H-)的结构示意图为 | |
| C. | 次氯酸的结构式为H-Cl-O | |
| D. | 中子数为19的钙离子为${\;}_{19}^{40}$Ca2+ |
17.某有机物的结构图,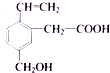 下列说法不正确的是( )
下列说法不正确的是( )
 下列说法不正确的是( )
下列说法不正确的是( )| A. | 能使Br2的四氯化碳溶液褪色 | B. | 能发生酯化反应 | ||
| C. | 该有机物的分子式C11H13O3 | D. | 能与金属钠发生反应 |
14.关于电池,以下叙述不正确的是( )
| A. | 化学电池的反应本质是氧化还原反应 | |
| B. | 最早使用的化学电池是锌锰电池 | |
| C. | 最早使用的充电电池是铅蓄电池 | |
| D. | 二次电池的放电反应与充电反应可能是可逆反应 |
1.下列可用于区别苯、甲苯、苯酚、四氯化碳四种无色液体的一组试剂为( )
| A. | 氯化铁溶液、溴水 | B. | NaOH溶液、溴水 | ||
| C. | NaHCO3溶液、溴水 | D. | 高锰酸钾溶液、溴水 |
18.下列说法正确的是( )
| A. | 在化学反应中一定有新物质生成,同时必有能量的释放 | |
| B. | 在化学反应中一定有新物质生成,但不一定有能量的变化 | |
| C. | 在化学反应中一定有化学键的变化 | |
| D. | 在化学反应中一定有化学键的变化,但不一定有能量的变化 |
19.将2molSO2和0.5molO2通入密闭容器中,充分反应后,容器中各物质的物质量关系一定正确的是( )
| A. | n(SO3)>n(SO2) | B. | n(SO3)=1mol | C. | 1mol<n(SO3)<2mol | D. | n(SO2)+n(SO3)=2mol |

 ,该反应类型为取代反应.
,该反应类型为取代反应. .
. .
. .
.