题目内容
13.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )| A. | 25℃时,1 L pH=1的H2SO4溶液中,SO${\;}_{4}^{2-}$数目为0.1NA | |
| B. | 将7.8 g Na2O2放入足量的CO2和水蒸气组成的气体中充分反应,转移电子总数为0.1NA | |
| C. | 9 g重氧水(H${\;}_{2}^{18}$O)含电子总数为10NA | |
| D. | 常温常压下,2.24 L正戊烷、异戊烷及新戊烷的混合物,含C-H数目为1.2NA |
分析 A、在硫酸溶液中,氢离子和硫酸根的物质的量之比为2;1;
B、求出过氧化钠的物质的量,然后根据过氧化钠和水或二氧化碳反应时,1mol过氧化钠转移1mol电子来分析;
C、求出重氧水的物质的量,然后根据重氧水中含10个电子来分析;
D、常温常压下气体摩尔体积大于22.4L/mol.
解答 解:A、pH=1的硫酸溶液中,氢离子浓度为0.1mol/L,故在1L溶液中含有的氢离子的物质的量为0.1mol,而在硫酸溶液中,氢离子和硫酸根的物质的量之比为2:1,故溶液中硫酸根的物质的量为0.05mol,个数为0.05NA个,故A错误;
B、7.8g过氧化钠的物质的量为0.1mol,而过氧化钠和水或二氧化碳反应时,1mol过氧化钠转移1mol电子,故0.1mol过氧化钠转移0.1NA个电子,故B正确;
C、9g重氧水H${\;}_{2}^{18}$O的物质的量n=$\frac{9g}{20g/mol}$=0.45mol,而重氧水中含10个电子,故0.45mol重氧水中含有4.5NA个电子,故C错误;
D、常温常压下气体摩尔体积大于22.4L/mol,故2.24L正戊烷、异戊烷和新戊烷的混合物的物质的量小于0.1mol,则含有的碳氢键个数小于1.2NA条,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
1.在200mL某硫酸盐Rm(SO4)n溶液中,含有1.5NA个SO42-和NA个R金属离子(NA表示阿伏加德罗常数),则该盐溶液的浓度为( )
| A. | 2.5 mol/L | B. | 5 mol/L | C. | 2 mol/L | D. | 7.5 mol/L |
8.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 12gC-13含有的原子数为NA | |
| B. | 28gCO和44gCO2含有的氧原子数均为NA | |
| C. | 1.7gH2O2中含有的电子数为0.9NA | |
| D. | 标准状况下,2.24LH2O所含分子数为0.1NA |
18.一定条件下,A、B、C的起始浓度分别是0.5mol/L、0.1mol/L、1.6mol/L,可逆反应A(g)+B(g)?2C(g)达到平衡时,下列数据不合理的是( )
| A. | c(A)=1.0mol/L c(B)=0.2mol/L | B. | c(B)=0.5mol/L c(C)=1.2mol/L | ||
| C. | c(A)=0.4mol/L c(C)=1.8mol/L | D. | c(A)=0.9mol/L c(B)=0.5mol/L |
5.某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NAMCON中自由移动.下列说法中正确的是( )


| A. | 传感器中通过的电流越大,CO的含量越低 | |
| B. | 工作时电子由电极a通过固体介质NAMCON流向电极b | |
| C. | 工作时电极b作正极,电流由电极a流向电极b | |
| D. | 当固体电解质中有1 mol O2-通过时,电子转移2 mol |
2.下列反应的离子方程式书写正确的是( )
| A. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 向CH3COOH溶液中加入CaCO3:2CH3COOH+CaCO3═2CH3COO-+Ca2++H2O+CO2↑ | |
| C. | 稀硫酸与Ba(OH)2溶液混合:H++SO42-+OH-+Ba2+═BaSO4↓+H2O | |
| D. | NaOH溶液与KHCO3溶液混合:OH-+HCO3-═H2O+CO2 |
3.水的电离平衡为H2O?H+﹢OH-,△H>0,下列叙述不正确的是( )
| A. | 将水加热,pH不变 | |
| B. | 恒温下,向水中加入少量固体KOH,c(OH-)变大 | |
| C. | 向水中滴入稀醋酸,c(H+)增大 | |
| D. | 向水中加入少量固体NaClO,平衡向右移动 |
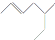 :5-甲基-2-庚烯,
:5-甲基-2-庚烯,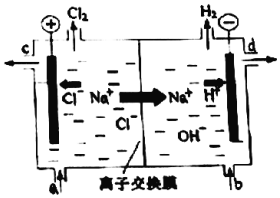 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源,进行惰性电极电解饱和氯化钠溶液实验.回答下列问题:
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源,进行惰性电极电解饱和氯化钠溶液实验.回答下列问题: