题目内容
三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
(1)反应过程中,被氧化与被还原的元素原子的物质的量之比为 .
(2)写出该反应的化学方程式 .若反应中生成0.2mol HNO3,转移的电子数目为 个.
(3)三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F 据题意推测 NF3,F2,NO三种气体中,氧化性由弱到强的顺序为
(4)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现.你判断该气体泄漏时的现象是 .
(5)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外,还肯定有 (填化学式).
(1)反应过程中,被氧化与被还原的元素原子的物质的量之比为
(2)写出该反应的化学方程式
(3)三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F 据题意推测 NF3,F2,NO三种气体中,氧化性由弱到强的顺序为
(4)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现.你判断该气体泄漏时的现象是
(5)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外,还肯定有
考点:氧化还原反应的计算,氧化性、还原性强弱的比较
专题:
分析:由反应物和生成物可写出反应的化学方程式为3NF3+5H2O=2NO+HNO3+9HF,反应中只有N元素的化合价发生变化,则氧化剂和还原剂都是NF3,NO易与空气中氧气反应生成红棕色的NO2气体,反应物可用碱液吸收.
解答:
解:(1)NF3→NO,化合价降低1价,被还原,NF3→HNO3,化合价升高2价,被氧化,氧化还原反应中氧化剂和还原剂得失电子数目相等,则被氧化与被还原的元素的物质的量之比为1:2,故答案为:1:2;
(2)由反应物和生成物可写出反应的化学方程式为3NF3+5H2O=2NO+HNO3+9HF,
由方程式可知若反应中生成0.2mol HNO3,转移的电子的物质的量为0.2mol×(5-3)=0.4mol,转移的电子数目为0.4NA个,
故答案为:3NF3+5H2O=2NO+HNO3+9HF;0.4NA;
(3)由4NH3+3F2=NF3+3NH4F可知氧化性F2>NF3,由3NF3+5H2O=2NO+HNO3+9HF可知氧化性NF3>NO,则氧化性F2>NF3>NO,故答案为:F2>NF3>NO;
(4)NO易与空气中氧气反应生成红棕色的NO2气体,同时生成的HF和HNO3易结合空气中的水蒸气形成酸雾,有刺激性气味,
故答案为:产生红棕色气体,产生刺激性气味气体,产生白雾;
(5)NF3与H2O反应产生HNO3,HNO3和NaOH反应必生成NaNO3,故答案为:NaNO3.
(2)由反应物和生成物可写出反应的化学方程式为3NF3+5H2O=2NO+HNO3+9HF,
由方程式可知若反应中生成0.2mol HNO3,转移的电子的物质的量为0.2mol×(5-3)=0.4mol,转移的电子数目为0.4NA个,
故答案为:3NF3+5H2O=2NO+HNO3+9HF;0.4NA;
(3)由4NH3+3F2=NF3+3NH4F可知氧化性F2>NF3,由3NF3+5H2O=2NO+HNO3+9HF可知氧化性NF3>NO,则氧化性F2>NF3>NO,故答案为:F2>NF3>NO;
(4)NO易与空气中氧气反应生成红棕色的NO2气体,同时生成的HF和HNO3易结合空气中的水蒸气形成酸雾,有刺激性气味,
故答案为:产生红棕色气体,产生刺激性气味气体,产生白雾;
(5)NF3与H2O反应产生HNO3,HNO3和NaOH反应必生成NaNO3,故答案为:NaNO3.
点评:本题考查含氮化合物的性质以及氧化还原反应,题目难度中等,注意从化合价变化的角度分析氧化还原反应的有关概念和计算,注意把握题给信息,为解答该题的关键.

练习册系列答案
相关题目
配制0.1mol/L盐酸溶液480mL,用量筒量取密度为1.19g/cm3质量分数为37%的浓盐酸约(取整数)( )mL注入烧杯中.用蒸馏水洗涤烧杯2~3次,将洗涤液注入容量瓶中.
| A、3.5 | B、3.8 |
| C、2.5 | D、4.2 |
下列说法正确的是( )
| A、硅元素主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| B、浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
| C、用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 |
| D、Ca(HCO3)2溶液与过量NaOH溶液反应可制得Ca(OH)2 |
下列判断中一定正确的是( )
| A、CaCl2及CaO2固体中阴、阳离子数之比均为2:1 |
| B、等质量的O2与O3中,氧原子的个数比为3:2 |
| C、分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1:2 |
| D、10mL 0.3mol?L-1NaCl与30mL0.1mol?L-1AlCl3溶液中Cl-物质的量浓度比为1:3 |
化学与日常生活密切相关,下列说法错误的是( )
| A、碘酒是指单质碘的乙醇溶液 |
| B、84消毒液的有效成分是NaClO |
| C、生石灰用作食品抗氧剂 |
| D、小苏打是面包发酵粉的主要成分 |
从结构上分析,有一种物质不同于其他三种,该物质是( )
A、 |
B、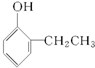 |
C、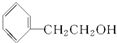 |
D、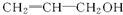 |
下列过程不涉及氧化还原反应的是( )
| A、二氧化氮气体冷却后颜色变浅 |
| B、镁条在二氧化碳气体中燃烧 |
| C、人工固氮 |
| D、久置的浓硝酸显黄色 |
下列物质中含分子数目最多的是( )
| A、0.1mol Cl2 |
| B、0.4g H2 |
| C、4℃时9mLH2O |
| D、标况下,6.72L CO2 |
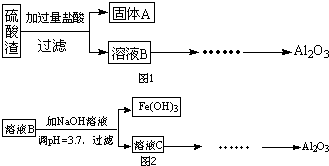 (1)写出溶液B的溶质是
(1)写出溶液B的溶质是