题目内容
 用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,
用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,| 实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
| 1 | 25.00 | 24.41 |
| 2 | 25.00 | 24.39 |
| 3 | 25.00 | 22.60 |
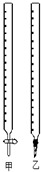
(1)如图中甲为
(2)取待测液NaOH溶液25.00mL于锥形瓶中,使用
(3)若滴定前,滴定管尖端有气泡,滴定后气泡消失,将使所测结果
(4)该NaOH溶液的物质的量浓度为
考点:中和滴定
专题:实验题
分析:(1)根据仪器的结构来分析;
(2)依据溶液的酸碱性来选择指示剂,根据溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(3)根据c(待测)=
来判断;
(4)先根据数据的有效性,然后求出平均消耗V(HCl),然后计算即可.
(2)依据溶液的酸碱性来选择指示剂,根据溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(3)根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
(4)先根据数据的有效性,然后求出平均消耗V(HCl),然后计算即可.
解答:
解:(1)甲滴定管的下端是玻璃活塞,所以仪器的名称为酸式滴定管,乙滴定管的下方是橡胶管,故名称为碱式滴定管,故答案为:酸式,碱式;
(2)碱溶液中滴加无色的酚酞,碱能使酚酞变红,故利用酚酞做指示剂,滴定达到终点的现象是:酚酞的红色褪去且半分钟不再出现红色,故答案为:酚酞,酚酞的红色褪去且半分钟不再出现红色;
(3)取标准液的滴定管,滴定前滴定管尖端有气泡,滴定后气泡消失,标准液的物质的量偏小,导致标准液的体积偏大,故根据c(待测)=
分析,C(待测)偏高;标准液读数时,若滴定前仰视,滴定后俯视,导致标准液的体积偏小,根据c(待测)=
分析,C(待测)偏低;故答案为:偏高;偏低;
(4)依据数据可知,舍去差距较大的22.60mL,故V(标准)=
=24.40mL,c(待测)=
=
=0.1288mol/L,故答案为:0.01288mol/L.
(2)碱溶液中滴加无色的酚酞,碱能使酚酞变红,故利用酚酞做指示剂,滴定达到终点的现象是:酚酞的红色褪去且半分钟不再出现红色,故答案为:酚酞,酚酞的红色褪去且半分钟不再出现红色;
(3)取标准液的滴定管,滴定前滴定管尖端有气泡,滴定后气泡消失,标准液的物质的量偏小,导致标准液的体积偏大,故根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
| V(标准)×c(标准) |
| V(待测) |
(4)依据数据可知,舍去差距较大的22.60mL,故V(标准)=
| 24.41+24.39 |
| 2 |
| V(标准)×c(标准) |
| V(待测) |
| 24.40mL×0.1320mol/L |
| 25.00mL |
点评:本题主要考查了滴定操作、注意事项以及误差分析,难度不大,特别注意数据的取舍,根据课本知识即可完成.

练习册系列答案
相关题目
下列试剂不会因为空气中的氧气而变质的是( )
| A、亚硫酸钠 | B、漂白粉 |
| C、硫酸亚铁 | D、氢硫酸 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、1mol CH4含有的电子数为NA |
| B、标准状况下,2.24L的CCl4中含有的氯原子数为0.4NA |
| C、常温常压下,3.0g葡萄糖和冰醋酸的混合物中含有的原子总数为0.4NA |
| D、标准状况下,2.24L的乙炔含碳原子数为0.4NA |
下列物质中的化学键类型与H2O相同的是( )
| A、C2H6 |
| B、HCl |
| C、NH4Cl |
| D、Na2O2 |
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如下表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如下表: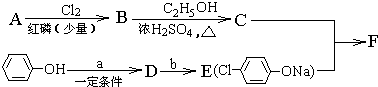
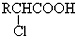 ,
,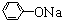 +RCl→
+RCl→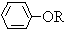 +NaCl
+NaCl