题目内容
把a L硫酸铵和硝酸铵混合液分为两等份,一份需用b mol烧碱刚好把氨气全部赶出(![]()
![]() NH3↑+H2O),另一份BaCl2溶液反应消耗c mol BaCl2,则原溶液中
NH3↑+H2O),另一份BaCl2溶液反应消耗c mol BaCl2,则原溶液中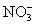 的物质的量浓度是
的物质的量浓度是
[ ]
A.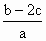 mol·L-1
mol·L-1
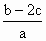 mol·L-1
mol·L-1B.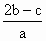 mol·L-1
mol·L-1
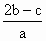 mol·L-1
mol·L-1C. mol·L-1
mol·L-1
 mol·L-1
mol·L-1D.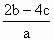 mol·L-1
mol·L-1
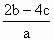 mol·L-1
mol·L-1
答案:D
解析:
解析:
|
由 |

练习册系列答案
相关题目
|
把 a L硫酸铵和硝酸铵的混合液分成两等份,一份加入b mol烧碱并加热,刚好把NH3全部赶出.另一份需消耗c mol BaCl2,沉淀反应刚好完全,原溶液中硝酸根离子的物质的量浓度为 | |
| [ ] | |
A. |
b-2c/a mol.l-1 |
B. |
2b-c/a mol.l-1 |
C. |
a-b/a mol.l-1 |
D. |
2b-4c/a mol.l-1 |
 +OH-=NH3↑+H2O可知,每一份中含n(
+OH-=NH3↑+H2O可知,每一份中含n( =BaSO4↓可知,每一份中含n(
=BaSO4↓可知,每一份中含n( )=n(
)=n( mol·L-1.
mol·L-1. mol.l-1 B.
mol.l-1 B. mol.l-1
mol.l-1 mol.l-1 D.
mol.l-1 D. mol.l-1
mol.l-1