题目内容
6.在原电池中,较活泼的金属组成的电极是负极,电池工作时这一极不断有电子流出,同时发生氧化反应;较不活泼的金属组成的电极是正极,电池工作时,这一极不断有电子流入,同时发生还原反应.分析 原电池中活泼金属失电子作负极,电子从负极流向正极,结合氧化还原反应分析.
解答 解:在原电池中,较活泼的金属组成的电极失电子是负极,电池工作时这一极不断有电子流出,同时发生氧化反应;较不活泼的金属组成的电极是正极,电池工作时,这一极不断有电子流 入,同时发生还原反应;
故答案为:负;出;氧化;正;入;还原.
点评 本题考查原电池知识,侧重于原电池的原理的应用的考查,注意把握原电池的正负极的判断以及发生的反应,难度不大.

练习册系列答案
相关题目
13.7瓶分别含有Cu2+、Fe3+、A13+、Mg2+、Fe2+、NH4+、Na+等离子的溶液,只用一种试剂即可鉴别,该试剂是( )
| A. | KMnO4溶液 | B. | KSCN溶液 | C. | NaOH溶液 | D. | NH3•H2O溶液 |
14.将足量的MnO2与含14.6gHCl的浓盐酸共热制取氯气,可制得Cl2的质量是( )
| A. | 等于7.1g | B. | 小于7.1g | ||
| C. | 大于7.1g,小于14.2g | D. | 大于14.2g |
1.取两份质量相等的有机物M,一份与足量的钠反应放出气体V1升,另一份与足量Na2CO3溶液反应放出气体V2升;若同温同压下V1>V2>0,则M可能是( )
| A. | CH3COOH | B. | HOOC-COOH | C. | HO(CH2)2CHO | D. | HO- -COOH -COOH |
11.某原电池装置如图所示,盐桥中装有用饱和氯化钾溶液浸泡过的琼脂.下列叙述正确的是( )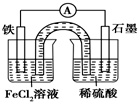

| A. | 原电池工作一段时间后,FeCl2溶液中c(Cl-)增大 | |
| B. | 此电池工作原理与硅太阳能电池工作原理相同 | |
| C. | Fe为正极,石墨上发生的反应为2H++2e-═H2↑ | |
| D. | 该装置中的盐桥完全可用金属导线代替 |
16.如图曲线a和b是盐酸与氢氧化钠相互滴定的滴定曲线,下列叙述正确的是( )


| A. | 盐酸的物质的量浓度为1mol/L | |
| B. | P点时恰好完全反应,溶液呈中性 | |
| C. | 曲线a是盐酸滴定氢氧化钠的滴定曲线 | |
| D. | 酚酞不能用作本实验的指示剂 |


 、
、 .
.