题目内容
在硫酸铜晶体(CuSO4?n H2O)结晶水含量测定的操作中,导致n值偏小的是
- A.晶体未研成粉末
- B.坩埚未干燥
- C.加热过程中晶体爆溅
- D.加热时间过长,部分变黑
A
分析:在硫酸铜晶体(CuSO4?n H2O)结晶水含量测定中,加热前后质量的减少量即是失去结晶水的质量,当晶体未研成粉末,导致晶体分解不完全,固体的质量差偏小;坩埚未干燥、加热过程中晶体爆溅、加热时间过长,部分变黑等而造成加热前后固体的质量差偏大,使n值偏大.
解答:A、晶体未研成粉末,导致晶体分解不完全,固体的质量差偏小,则n值偏小,故A正确;
B、坩埚未干燥,加热后水挥发,而造成加热前后固体的质量差偏大,使n值偏大,故B错误;
C、加热过程中晶体爆溅,而造成加热前后固体的质量差偏大,使n值偏大,故C错误;
D、加热时间过长,部分变黑等都将导致硫酸铜分解固体变黑说明硫酸铜分解生成CuO与SO3,故m(H2O)偏大,
m(CuSO4)偏小,而造成加热前后固体的质量差偏大,使n值偏大,故D错误;
故选A.
点评:本题考查硫酸铜晶体中结晶水的测定,把握实验操作时的注意事项,分析误差时从导致加热前后的质量差进行判断.
分析:在硫酸铜晶体(CuSO4?n H2O)结晶水含量测定中,加热前后质量的减少量即是失去结晶水的质量,当晶体未研成粉末,导致晶体分解不完全,固体的质量差偏小;坩埚未干燥、加热过程中晶体爆溅、加热时间过长,部分变黑等而造成加热前后固体的质量差偏大,使n值偏大.
解答:A、晶体未研成粉末,导致晶体分解不完全,固体的质量差偏小,则n值偏小,故A正确;
B、坩埚未干燥,加热后水挥发,而造成加热前后固体的质量差偏大,使n值偏大,故B错误;
C、加热过程中晶体爆溅,而造成加热前后固体的质量差偏大,使n值偏大,故C错误;
D、加热时间过长,部分变黑等都将导致硫酸铜分解固体变黑说明硫酸铜分解生成CuO与SO3,故m(H2O)偏大,
m(CuSO4)偏小,而造成加热前后固体的质量差偏大,使n值偏大,故D错误;
故选A.
点评:本题考查硫酸铜晶体中结晶水的测定,把握实验操作时的注意事项,分析误差时从导致加热前后的质量差进行判断.

练习册系列答案
相关题目
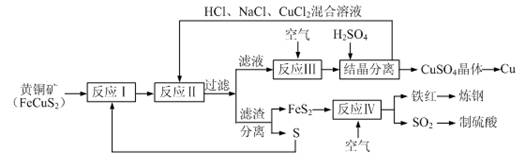
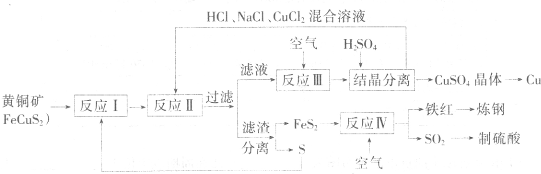
【化学——选修化学与技术】(15分)现有一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下:
注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl—=2[CuCl2]-+S
请回答下列问题:
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。这种方法的缺点是 _____________________ ________、___________________________________ 。
(2)反应Ⅰ的产物为(填化学式) ___________________ 。
(3)反应Ⅲ的离子方程式为 ____________________________________________________ 。
(4)一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是 ___________
(5)黄铜矿中Fe的化合价为+2,对于反应:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是 ___________________ (填字母)。
8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是 ___________________ (填字母)。
| A.反应中被还原的元素只有氧 | B.反应生成的SO2直接排放会污染环境 |
| C.SO2既是氧化产物又是还原产物 | D.当有8mol铜生成时,转移电子数目为100NA |
已知:Cr2O72-+ Fe2++ H+→Cr3++ Fe3++ H2O(未配平)
①SO2通入Fe2(SO4)3溶液,发生反应的离子方程式为 ____________________________________ 。
②反应Ⅳ所得气体中SO2的体积分数为________________________________________________ 。

 8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是 ___________________ (填字母)。
8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是 ___________________ (填字母)。