题目内容
14.用NA代表阿伏加德罗常数,下列叙述正确的是( )| A. | 78g Na2O2中含有的离子总数为4NA | |
| B. | 标准状况下,1.12L HF中所含的分子总数为0.05NA | |
| C. | 由CO2和O2组成的混合物共有NA个分子,其中的氧原子数为2NA | |
| D. | 0.11mol•L-1 FeCl3溶液中含有的Cl-数目为0.3NA |
分析 A、求出过氧化钠的物质的量,然后根据过氧化钠由2个钠离子和1个过氧根构成来分析;
B、标况下HF为液体;
C、二氧化碳和氧气中均含2个氧原子;
D、溶液体积不明确.
解答 解:A、78g过氧化钠的物质的量为1mol,而过氧化钠由2个钠离子和1个过氧根构成,故1mol过氧化钠中含3NA个离子,故A错误;
B、标况下HF为液体,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、二氧化碳和氧气中均含2个氧原子,故NA个混合物分子中含有的氧原子为2NA个,故C正确;
D、溶液体积不明确,故溶液中的氯离子的个数无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
16.在下列变化中需加入还原剂才能实现的是( )
| A. | KClO3→HCl | B. | Na2O2→O2 | C. | Fe Cl3→FeCl2 | D. | SO2→SO3 |
5.金刚石和石墨是碳元素的两种结构不同的单质,在101kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的能量.下列说法不正确的是( )
| A. | 石墨比金刚石稳定 | |
| B. | 金刚石转化为石墨是物理变化 | |
| C. | 1 mol金刚石比1 mol石墨的总能量高 | |
| D. | 1 mol石墨和1 mol金刚石完全燃烧时释放的能量,石墨比金刚石少 |
2.下列各组液体混合物能用分液漏斗分离的是( )
| A. | 乙酸和水 | B. | 乙醇和水 | C. | 乙醇和乙酸 | D. | 苯和水 |
9.25℃时,0.1mol/L CH3COOH溶液的pH( )
| A. | =1 | B. | >1 | C. | <1 | D. | =0 |
19.图中,R、W、X、Y、Z为元素周期表中前四周期的部分元素,下列有关叙述正确的是( )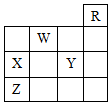

| A. | 五种元素中,只有Z为金属元素 | |
| B. | W位于ⅥA族,有+6、-2两种常见化合价 | |
| C. | X和Y的最高价氧化物对应水化物都是强酸 | |
| D. | X、Y、Z的气态氢化物的稳定性:Y>X>Z |
6.用提供的试剂(溴水、浓硝酸、碘水、新制氢氧化铜浊液)分别鉴别下列有机物,将所用试剂及产生的现象的序号填在横线上.
| 序号 | 待鉴别的物质 | 试剂 | 现象 |
| ① | 乙烯 | 溴水 | 橙色褪去 |
| ② | 葡萄糖 | 新制氢氧化铜浊液 | 出现砖红色沉淀 |
| ③ | 淀粉 | 碘水 | 溶液呈蓝色 |
3. 关于元素铬(Cr)的信息如下:
关于元素铬(Cr)的信息如下:
Ⅰ.
Ⅱ.Cr(OH)3为难溶于水的灰蓝色固体
Ⅲ.CrO42-和Cr2O72-在溶液中可相互转化:2CrO42-+2H+?Cr2O72-+H2O
室温下,初始浓度为1.0mol•L-1的Na2CrO4溶液中c(Cr2O72-)随c(H+)的变化如图所示,以下说法正确的是( )
 关于元素铬(Cr)的信息如下:
关于元素铬(Cr)的信息如下:Ⅰ.
| 溶液中存在形式 | Cr3+ | Cr(OH)4- ( 可写成CrO2-) | Cr2O72- | CrO42- |
| 颜色 | 蓝紫色 | 绿色 | 橙红色 | 黄色 |
Ⅲ.CrO42-和Cr2O72-在溶液中可相互转化:2CrO42-+2H+?Cr2O72-+H2O
室温下,初始浓度为1.0mol•L-1的Na2CrO4溶液中c(Cr2O72-)随c(H+)的变化如图所示,以下说法正确的是( )
| A. | 若已知Cr3+与Al3+的化学性质相似,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到产生灰蓝色沉淀,然后沉淀逐渐溶解形成无色溶液 | |
| B. | 由图可知,溶液酸性增大,CrO42-的平衡转化率减小 | |
| C. | 根据A点数据,可计算出该转化反应的平衡常数为2×1.0×1014 | |
| D. | B点溶液中,3c (Cr2O72-)=c (CrO42-) |
17.根据元素周期表推测Fe元素在周期表中位于第四周期( )
| A. | 第ⅢB族 | B. | 第Ⅲ族 | C. | 第VⅢ族 | D. | 第VⅢB族 |