题目内容
18.下列离子方程式正确的是( )| A. | 向硫酸铝铵溶液中滴加少量Ba(OH)2溶液:NH${\;}_{4}^{+}$+Al3++2SO${\;}_{4}^{2-}$+2Ba2++5OH-═AlO+2BaSO4↓+NH3•H2O+2H2O | |
| B. | 工业上用石灰乳制备漂白粉:Ca(OH)2+Cl2═Ca2++ClO-+Cl-+H2O | |
| C. | 制备Fe(OH)3胶体:Fe3++3H2O?Fe(OH)3(胶体)+3H+ | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
分析 A.少量Ba(OH)2完全反应,反应生成硫酸钡、氢氧化铝和一水合氨;
B.石灰乳中的氢氧化钙需要保留化学式;
C.该反应用等号连接,且需要加热;
D.酸性高锰酸钾溶液能够氧化盐酸中的氯离子,干扰了检验.
解答 解:A.少量Ba(OH)2完全反应,反应生成硫酸钡、氢氧化铝,正确的离子反应为:2Al3++3SO42-+3Ba2++6OH═3BaSO4↓+2Al(OH)3↓,故A错误;
B.工业上用石灰乳制备漂白粉,反应的离子方程式为:Ca(OH)2+Cl2═Ca2++ClO-+Cl-+H2O,故B正确;
C.制备Fe(OH)3胶体的反应需要加热,不能用可逆号,正确的离子方程式为:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3H+,故C错误;
D.酸性高锰酸钾溶液检验强氧化性,能够氧化氯离子,不能用浓盐酸酸化,可以用稀硫酸酸化,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等;D为易错点,注意酸性高锰酸钾能够氧化氯离子,需要用硫酸酸化.

练习册系列答案
相关题目
8.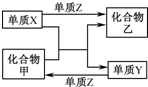 X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物.下表各组物质之间通过一步反应不能实现如图所示转化的是( )
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物.下表各组物质之间通过一步反应不能实现如图所示转化的是( )
 X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物.下表各组物质之间通过一步反应不能实现如图所示转化的是( )
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物.下表各组物质之间通过一步反应不能实现如图所示转化的是( )| 选项 | X | Y | Z | 甲 | 乙 |
| A | Fe | H2 | O2 | H2O | Fe3O4 |
| B | Mg | C | O2 | CO2 | MgO |
| C | Zn | Fe | Cl2 | FeCl2 | ZnCl2 |
| D | Cl2 | N2 | H2 | NH3 | HCl |
| A. | A | B. | B | C. | C | D. | D |
6.一定条件下进行反应:COCl2(g)?Cl2(g)+CO(g),向2.0L恒容密闭容器中充入1.0mol COCl2(g),经过一段时间后达到平衡.反应过程中测得的有关数据见表:
下列说法正确的是(
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A. | 保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol•L-1,则反应的△H<0 | |
| B. | 若在2 L恒容绝热(与外界无热量交换)密闭容器中进行该反应,化学平衡常数改变 | |
| C. | 保持其他条件不变,起始向容器中充入1.2 molCOCl2、0.60 molCl2和0.60 molCO, 反应达到平衡前的速率:v(正)>v(逆) | |
| D. | 保持其他条件不变,起始向容器中充入1.0 molCl2和0.8 molCO,达到平衡时,Cl2的转化率小于60% |
3.某溶液中含有MgCl2的浓度为2mol.L-1,含AlCl3的浓度为3mol.L-1,体积为200mL,将此溶液中的Mg2+转化为沉淀分离出来,至少需要4mol.L-1的NaOH溶液的体积是( )
| A. | 0.2L | B. | 0.5L | C. | 0.65L | D. | 0.8L |
10.下列离子反应方程式正确的是( )
| A. | 向Ca(HCO3)2溶液加入过量的NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| B. | 向NH4HCO3溶液中滴入少量NaOH溶液:NH4++OH-═NH3•H2O | |
| C. | FeSO4溶液在空气中变黄色:4Fe2++O2+4H+═4Fe3++2H2O | |
| D. | 用NaOH溶液吸收NO2气体:3NO2+2NaOH═2NaNO3+NO↑+H2O |
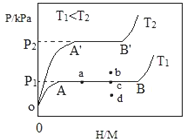 合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用.
合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用.