题目内容
13. 如表各组物质中,不能通过一步反应实现如图所示转化的是( )
如表各组物质中,不能通过一步反应实现如图所示转化的是( )| 选项 | X | Y | Z |
| A | Fe | FeCl3 | FeCl2 |
| B | NH4Cl | NH3 | NO |
| C | C | CO | CO2 |
| D | Al2O3 | AlCl3 | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Fe与氯气反应生成FeCl3,FeCl3与Fe反应生成FeCl2,FeCl2可与Zn等反应生成Fe;
B.NO不能直接生成NH4Cl;
C.C可氧气反应CO,进一步反应生成CO2,CO2和Mg反应可生成C;
D.氧化铝和盐酸反应生成氯化铝,氯化铝和碱反应生成氢氧化铝,氢氧化铝加热分解可生成氧化铝.
解答 解:A.2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3、2FeCl3+Fe=3FeCl2、2FeCl2+Cl2=2FeCl3、FeCl2+Zn=ZnCl2+Fe,故A正确;
B.NO不能直接生成NH4Cl,故B错误;
C.C完全燃烧生成CO2,不完全燃烧生成CO,CO继续燃烧生成CO2,CO2与Mg反应生成C,故C正确;
D.Al2O3+6HCl=2AlCl3+3H2O、AlCl3+3NH3.H2O=Al(OH)3↓+3NH4Cl、Al(OH)3+3HCl=AlCl3+3H2O、2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O,故D正确.
故选B.
点评 本题考查了物质间的转化,为高频考点,明确物质的性质是解本题关键,注意反应物相同,反应条件不同、反应物的量不同,产物可能不同,为易错点,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
3.常温下,下列各组离子在指定的溶液中可能大量共存的是( )
| A. | 无色透明溶液中:Al3+、Ca2+、Cl-、HCO3- | |
| B. | 含大量Fe3+的溶液中:K+、I-、SO42-、NO3- | |
| C. | 由水电离出的c(H+)=1.0×10-14 mol•L-1的溶液中:Mg2+、K+、Cl-、SO42- | |
| D. | 与Al反应放出H2的溶液中:NH4+、Na+、NO3-、F- |
1.在天平两边各放一只盛有相同浓度、相同体积的足量盐酸溶液的烧杯,调节天平到平衡,在左边烧杯中放入3.6的铝粉,为使天平最终保持平衡,右边烧杯中应放入镁粉的量是( )
| A. | 3.49g | B. | 3.60g | C. | 3.81g | D. | 3.92g |
8.可逆反应:N2(g)+3H2(g)?2NH3(g)的正逆反应速率可用反应物或生成物的浓度变化来表示,下列各关系中能说明反应已达平衡状态的是( )
| A. | v正(N2)=v正(H2) | B. | v正(N2)=v逆(NH3) | ||
| C. | 2 v正(H2)=3 v逆(NH3) | D. | v正(N2)=v逆(H2) |
5.已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeC12溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在KI-淀粉试纸上,试纸变蓝色.下列判断正确的是( )
| A. | 实验①生成的气体不能使湿润的KI-淀粉试纸变蓝 | |
| B. | 实验②证明Fe2+既有氧化性又有还原性 | |
| C. | 上述实验证明氧化性:MnO4->CI2>Fe3+>I2 | |
| D. | 上述实验中,共有两个氧化还原反应 |
11. 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.
(1)Y原子核外共有7种不同运动状态的电子,基态T原子有7种不同能级的电子.
(2)X、Y、Z的第一电离能由小到大的顺序为C<O<N(用元素符号表示).
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为sp杂化.
(4)Z与R能形成化合物甲,1mol甲中含4 mol化学键,甲与氢氟酸反应,生成物的分子空间构型分别为SiF4为正四面体形、H2O为V形.
(5)G、Q、R氟化物的熔点如表,造成熔点差异的原因为NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低;Mg2+的半径比Na+的半径小、电荷数高,晶格能MgF2>NaF,故MgF2的熔点比NaF高.
(6)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应的离子方程式为Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-
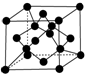
(7)X单质的晶胞如图所示,一个X晶胞中有8个X原子;若X晶体的密度为ρ g•cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个X原子之间的距离为$\frac{\sqrt{3}}{4}×\root{3}{\frac{96}{ρ{N}_{A}}}$ cm(用代数式表示).
 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.(1)Y原子核外共有7种不同运动状态的电子,基态T原子有7种不同能级的电子.
(2)X、Y、Z的第一电离能由小到大的顺序为C<O<N(用元素符号表示).
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为sp杂化.
(4)Z与R能形成化合物甲,1mol甲中含4 mol化学键,甲与氢氟酸反应,生成物的分子空间构型分别为SiF4为正四面体形、H2O为V形.
(5)G、Q、R氟化物的熔点如表,造成熔点差异的原因为NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低;Mg2+的半径比Na+的半径小、电荷数高,晶格能MgF2>NaF,故MgF2的熔点比NaF高.
| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1 539 | 183 |
(7)X单质的晶胞如图所示,一个X晶胞中有8个X原子;若X晶体的密度为ρ g•cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个X原子之间的距离为$\frac{\sqrt{3}}{4}×\root{3}{\frac{96}{ρ{N}_{A}}}$ cm(用代数式表示).