题目内容
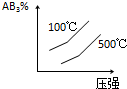
已知反应A2(g)+2B2(g)?2AB2(g)(正反应放热),下列说法正确的( )
| A.升高温度,正向反应速率减小,逆向反应速率增加 |
| B.升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
| D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
解;A、升高温度,正向反应速率、逆向反应速率均增加,故A错误;
B、升高温度有利于反应速率增加,从而缩短达到平衡的时间,故B正确;
C、达到平衡后,升高温度,平衡向着逆向进行,增大压强平衡正向移动,故C错误;
D、达到平衡后,降低温度或增大压强都有利于该反应平衡正向移动,故D错误.
故选B.
B、升高温度有利于反应速率增加,从而缩短达到平衡的时间,故B正确;
C、达到平衡后,升高温度,平衡向着逆向进行,增大压强平衡正向移动,故C错误;
D、达到平衡后,降低温度或增大压强都有利于该反应平衡正向移动,故D错误.
故选B.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目