题目内容
16.设NA是阿伏伽德罗常数的值,下列说法正确的是( )| A. | 4.6g NO2(g)和N2O4(g)的混合物中含有0.3NA个原子 | |
| B. | 0.1mol乙酸与足量乙醇发生酯化反应,生成0.1NA个乙酸乙酯分子 | |
| C. | 常温下将5.6gFe投入足量浓硫酸,电子转移数为0.3NA | |
| D. | Na2O2与足量H2O发生反应,每生成2.24L气体(标准状况),电子转移数0.4NA |
分析 A、NO2与N2O4的最简式均为NO2;
B、酯化反应为可逆反应;
C、根据常温下铁与浓硝酸发生钝化判断;
D、过氧化钠中氧元素的化合价为-1价,则生成1mol氧气转移了2mol电子.
解答 解:A、NO2与N2O4的最简式均为NO2,故4.6g混合物中含有的NO2的物质的量为0.1mol,则含0.3NA个原子,故A正确;
B、酯化反应为可逆反应,不能进行彻底,故生成的乙酸乙酯的分子个数小于0.1NA个,故B错误;
C、由于常温下铁与浓硝酸发生钝化,阻止了反应的进行,故C错误;
D、n(O2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,过氧化钠中氧元素的化合价为-1价,则生成1mol氧气转移了2mol电子,故则生成0.1mol氧气转移了0.2mol电子.转移电子的数目为0.2NA,故D错误,
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
6.对于放热反应A2+B2═C2,下列说法正确的是( )
| A. | 产物C2所具有的总能量高于反应物A2和B2所具有的总能量 | |
| B. | 反应物A2和B2所具有的总能量高于产物C2所具有的总能量 | |
| C. | 破坏A2和B2分子内的化学键所吸收的总能量高于形成C2分子内的化学键所放出的总能量 | |
| D. | 破坏A2和B2分子内的化学键所放出的总能量高于形成C2分子内的化学键所吸收的总能量 |
7.实验室以蛇纹石酸浸出液(主要含Fe3+,还有一定量的Al3+、Mn2+、Ca2+、Mg2+等)为原料制备高纯氧化铁,流程如图1:
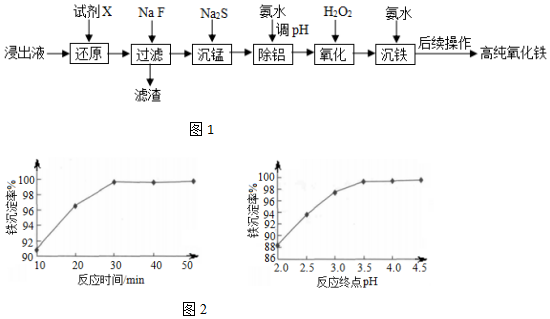
已知流程中相关金属离子生成氢氧化物沉淀的pH如表:
(1)“还原”时,应选择C(填字母).
A.Zn粉 B.NaClO溶液 C.Fe粉
(2)“滤渣”的主要成分除含有少量MnF2外,还含有CaF2、MgF2(填化学式).
(3)“沉锰”时,已知:Ksp(MnS)=4.65×10-14.为确保沉锰完全[即溶液中c(Mn2+)<1.0×10-6 mol•L-1],应保持溶液中c(S2-)>4.65×10-8mol•L-1mol•L-1.
(4)“除铝”时,控制溶液pH的范围为5.0~5.8.
(5)“氧化”时,常用酸性K2Cr2O7溶液检测是否残留未被氧化的金属离子,该反应的离子方程式为Cr2O72-+14H++6Fe2+═2Cr3++6Fe3++7H2O.
(6)“沉铁”时,反应温度为85℃条件下,反应时间和反应终点pH对铁的沉淀率的影响分别如图2所示,则最佳的工艺条件是反应时间30min、终点pH=3.5.

已知流程中相关金属离子生成氢氧化物沉淀的pH如表:
| 氢氧化物 | Fe3+ | Fe2+ | Al3+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 |
| 沉淀完全的pH | 3.2 | 8.8 | 5.0 |
A.Zn粉 B.NaClO溶液 C.Fe粉
(2)“滤渣”的主要成分除含有少量MnF2外,还含有CaF2、MgF2(填化学式).
(3)“沉锰”时,已知:Ksp(MnS)=4.65×10-14.为确保沉锰完全[即溶液中c(Mn2+)<1.0×10-6 mol•L-1],应保持溶液中c(S2-)>4.65×10-8mol•L-1mol•L-1.
(4)“除铝”时,控制溶液pH的范围为5.0~5.8.
(5)“氧化”时,常用酸性K2Cr2O7溶液检测是否残留未被氧化的金属离子,该反应的离子方程式为Cr2O72-+14H++6Fe2+═2Cr3++6Fe3++7H2O.
(6)“沉铁”时,反应温度为85℃条件下,反应时间和反应终点pH对铁的沉淀率的影响分别如图2所示,则最佳的工艺条件是反应时间30min、终点pH=3.5.
4.设NA为阿伏加德罗常数的数值,下列说法错误的是( )
| A. | 标准状况下,11.2L己烷中含有的碳碳键数为2.5NA | |
| B. | 2molNO和1molO2在密闭容器中充分反应,反应后容器中的分子数小于2NA | |
| C. | 由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA | |
| D. | 1molNa与O2完全反应.生成Na2O和Na2O2的混合物,转移电子总数为NA |
11.下列实验现象和结论相对应且正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 证明该溶液中存在Na+、不含K+ |
| B | 用浓盐酸和石灰石反应声生的气体直接通入Na2SiO3溶液中 | Na2SiO3溶液变浑浊 | C元素的非金属性大于Si元素 |
| C | 将石蜡油在碎瓷片上加热,产生的气体通过酸性KMnO4溶液 | 酸性KMnO4溶液紫红色褪去 | 石蜡油分解产生了不同于烷烃的气体,且该气体具有还原性 |
| D | 某溶液加入稀硝酸酸化的BaCl2溶液 | 产生白色沉淀 | 该溶液中一定存在SO42-或者Ag+ |
| A. | A | B. | B | C. | C | D. | D |
1.下列有关叙述正确的是( )
| A. | XX化妆品从纯天然植物中提取,不含任何化学物质 | |
| B. | 红宝石、玛瑙、水晶、钻石等制作装饰品的材枓,其物质的主要成份都是硅酸盐 | |
| C. | 氢氧燃料电池、硅太阳能电池中都利用了原电池原理 | |
| D. | 镧镍合金能大量吸收H2形成金属氢化物,可作储氢材科 |
18.若把元素周期表原来的主副族及族号取消,从左到右共有18列,则下列说法中错误的是( )
| A. | 第17列为卤族元素 | |
| B. | 第9列元素中没有非金属元素 | |
| C. | 只有第2列元素原子的最外层有2个电子 | |
| D. | 在整个18列元素中,第3列元素种类最多 |
19.化学与科学、技术、社会、环境密切相关.下到有关说法不正确的是( )
| A. | 光导纤维的主要成分是SiO2,太阳能电池的主要成分是单质硅 | |
| B. | 墨水是一种胶体,不同墨水混用时可能使铭笔流水不畅或者堵塞 | |
| C. | 食品包装袋内常用硅胶、生石灰和还原铁粉,其作用相同 | |
| D. | 用铝制容器盛装浓硫酸的原因是其表面发生钝化反应 |