题目内容
根据下列金属的熔沸点其中不能形成合金的是( )
| 金属 | Na | Cu | Al | Fe |
| 熔点(℃) | 97.5 | 1 083 | 660 | 1 535 |
| 沸点(℃) | 883 | 2 595 | 2 200 | 3 000 |
| A、Cu与Al |
| B、Fe与Cu |
| C、Fe与Na |
| D、Al与Na |
考点:合金的概念及其重要应用
专题:金属概论与碱元素
分析:由合金的形成可知,两种金属若能够形成合金,则熔点较高的金属的熔点不能大于熔点较低的金属的沸点.
解答:
解:合金是不同种金属在熔化状态下形成的一种熔合物,即两种金属都成为液态时进行混合;
A.铜的熔点低于铝的沸点,两种金属能够形成合金,故A错误;
B.铁的熔点低于铜的沸点,两种金属能够形成合金,故B错误;
C.由于金属钠的沸点较低,铁的熔点高于钠的沸点,在铁熔化时温度达1535℃,而此时金属钠已变成气态,无法完成液态时混合,故钠和铁不能形成合金,故C正确;
D.铝的熔点低于钠的沸点,两种金属能够形成合金,故D错误;
故选C.
A.铜的熔点低于铝的沸点,两种金属能够形成合金,故A错误;
B.铁的熔点低于铜的沸点,两种金属能够形成合金,故B错误;
C.由于金属钠的沸点较低,铁的熔点高于钠的沸点,在铁熔化时温度达1535℃,而此时金属钠已变成气态,无法完成液态时混合,故钠和铁不能形成合金,故C正确;
D.铝的熔点低于钠的沸点,两种金属能够形成合金,故D错误;
故选C.
点评:本题考查了合金的形成条件,题目难度不大,注意制造合金时,两种金属必须都是液态才能制成合金,一种液态、一种气态不会转化成合金.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
荧光素(X)常用于钞票等防伪印刷,下列关于它的说法正确的是( )
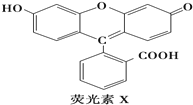

| A、1molX与足量的NaOH溶液在常温常压下反应,最多消耗3molNaOH |
| B、1molX最多能与9mol氢气反应 |
C、X能与糠醛(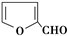 )发生缩聚反应 )发生缩聚反应 |
| D、1molX与足量的浓溴水反应,最多消耗4molBr2 |
已知反应:①Cl2+2KBr=2KCl+Br2;②KClO3+6HCl=3Cl2↑+KCl+3H2O;③2KBrO3+Cl2=Br2+2KClO3下列说法错误的是( )
| A、氧化性由强到弱的顺序为KBrO3>KClO3>Cl2>Br2 |
| B、①中KCl是氧化产物,KBr 发生还原反应 |
| C、③中2mol氧化剂参加反应得到电子的物质的量为10 mol |
| D、反应②中氧化剂与还原剂的物质的量之比为1:6 |
下列叙述不正确的是( )
| A、光照氯水有气泡逸出,该气体是Cl2 |
| B、工业上可用碳在高温下还原二氧化硅制取硅 |
| C、工业上可用氯气和石灰乳为原料制造漂白粉 |
| D、将盛有氢氧化铁胶体的烧杯置于暗处,用一束光照射,从垂直于光线的方向可以观察到一条光亮的通路 |
下列说法中不正确的是( )
| A、大型中央空调的制冷剂可用液氨 |
| B、工业上用H2和N2合成氨与自然界中放电时O2和N2反应都属于氮的固定 |
| C、常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
| D、铵盐易溶于水,且可与强碱发生复分解反应 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B、常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| C、某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
| D、标准状态下,33.6L氟化氢中含有氟原子的数目为1.5NA |
分类法在化学学科的发展中起到非常重要的作用,下列分类标准合理的是( )
| A、根据酸分子中含有的H原子个数将酸分为一元酸,二元酸和多元酸 |
| B、根据反应中是否有离子参加化学反应分为离子反应和非离子反应 |
| C、根据水溶液是否能够导电,将物质分为电解质和非电解质 |
| D、根据是否含有氧元素,将物质分为氧化剂和还原剂 |