题目内容
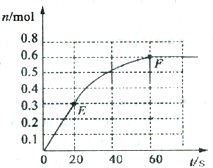 373K时,某1L恒容密闭容器中加入1molNH3,发生如下可逆反应2NH3(g)?N2(g)+3H2(g).其中物质H2的物质的量随时间变化如图所示.
373K时,某1L恒容密闭容器中加入1molNH3,发生如下可逆反应2NH3(g)?N2(g)+3H2(g).其中物质H2的物质的量随时间变化如图所示.(1)前 20 s内NH3(g)的平均反应速率为
(2)373K时该反应的平衡常数的值为
(3)若在此平衡体系中再加入 1mol的NH3,与原平衡比较,新平衡时 NH3的转化率
考点:反应速率的定量表示方法,化学平衡的影响因素,化学平衡的计算
专题:
分析:(1)根据化学反应速率的定义和化学反应速率之比等化学计量数之比进行计算;
(2)平衡常数k=
,利用三段式解题法,求出平衡时混合物各组分的物质的量,体积为1L,用物质的量代替浓度代入k进行计算;
(3)平衡体系中再加入1mol的氨气,重新到达平衡状态,可以等效为开始加入2mol的氨气,压强增大为原来的2倍,平衡向体积减小的方向移动,即向逆反应方向移动,转化率降低,NH3的平衡浓度增大.
(2)平衡常数k=
| c(N2)?c2(H2) |
| c2(NH3) |
(3)平衡体系中再加入1mol的氨气,重新到达平衡状态,可以等效为开始加入2mol的氨气,压强增大为原来的2倍,平衡向体积减小的方向移动,即向逆反应方向移动,转化率降低,NH3的平衡浓度增大.
解答:
解:2NH3(g)?N2(g)+3H2(g),
(1)20s内氢气的物质的量增加0.3mol,故氨气的物质的量减少
×2=0.2mol,故前 20s内v(NH3)=
=0.01(mol/L?s),
故答案为:0.01(mol/L?s);
(2)由图象可知60s时,反应达平衡,平衡时生成的氢气的物质的量为0.6mol,
2NH3(g)?N2(g)+3H2(g),
开始(mol):1 0 0
变化(mol):0.4 0.2 0.6
平衡(mol):0.6 0.2 0.6
所以k=
=
=0.12,
故答案为:0.12;
(3)平衡体系中再加入1mol的氨气,重新到达平衡状态,可以等效为开始加入2mol的氨气,压强增大为原来的2倍,平衡向体积减小的方向移动,即向逆反应方向移动,转化率降低,NH3的平衡浓度增大,
故答案为:减小;增大.
(1)20s内氢气的物质的量增加0.3mol,故氨气的物质的量减少
| 0.3 |
| 3 |
| ||
| 20s |
故答案为:0.01(mol/L?s);
(2)由图象可知60s时,反应达平衡,平衡时生成的氢气的物质的量为0.6mol,
2NH3(g)?N2(g)+3H2(g),
开始(mol):1 0 0
变化(mol):0.4 0.2 0.6
平衡(mol):0.6 0.2 0.6
所以k=
| c(N2)?c2(H2) |
| c2(NH3) |
| 0.2×(0.6)3 |
| (0.6)2 |
故答案为:0.12;
(3)平衡体系中再加入1mol的氨气,重新到达平衡状态,可以等效为开始加入2mol的氨气,压强增大为原来的2倍,平衡向体积减小的方向移动,即向逆反应方向移动,转化率降低,NH3的平衡浓度增大,
故答案为:减小;增大.
点评:本题考查化学反应速率的计算,化学平衡平衡常数的计算及等效平衡思想的利用,难度中等.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
某学生的实验报告所列出的下列数据中合理的是( )
| A、用10mL量筒量取8.16mL稀盐酸 |
| B、用托盘天平称取25.20gNaCl |
| C、用广泛pH试纸测得某溶液的pH为2.3 |
| D、用25mL碱式滴定管进行中和滴定时,用去某浓度的碱溶液21.70mL |
下列各离子组中,一定能大量共存的一组是( )
| A、pH=1的溶液中:Fe2+、Cl-、Na+、NO3- |
| B、由水电离出的c(H+)=1×10-13mol/L溶液中:Na+、CO32-、Cl-、K+ |
| C、pH=7的溶液中:NH4+、HCO3-、Mg2+、SO42- |
| D、无色溶液中:Al3+、HCO3-、I-、Ca2+ |
化学与生产、生活密切相关.下列叙述正确的是( )
| A、二氧化硫的大量排放是造成光化学烟雾的主要原因 |
| B、使用清洁能源是防止酸雨发生的重要措施之一 |
| C、使用无磷洗衣粉,可彻底解决水体富营养化问题 |
| D、某雨水样品放置一段时间后pH减小是因为水中溶解的CO2增多 |
0.1mol/L CH3COOH溶液中加水或加入少量CH3COONa晶体时,都会引起的变化的是( )
| A、溶液的pH增大 |
| B、CH3COOH的电离程度变大 |
| C、溶液的导电能力减弱 |
| D、溶液中c(OH-)减少 |