题目内容
19.(1)现有三组混合液:①乙酸乙酯和乙酸钠溶液 ②乙醇和丁醇 ③溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是③.①分液、萃取、蒸馏 ②萃取、蒸馏、分液 ③分液、蒸馏、萃取 ④蒸馏、萃取、分液
(2)鉴别己烷、己烯、甲苯、溴乙烷、乙酸溶液和乙醇6种无色液体,可选用的最佳试剂组合是C
A.酸性KMnO4溶液、溴水B.金属钠、溴水、石蕊试液
C.石蕊试液、溴水D.酸性KMnO4溶液、石蕊试液
(3)分子式为C3H6O2的二元混合物,如果在核磁共振氢谱上观察到氢原子给出的峰有两种情况.第一种情况峰给出的强度为1:1;第二种情况峰给出的强度为3:2:1.由此推断混合物的组成可能是CH3COOCH3、HCOOCH2CH3或CH3COOCH3、HCOOCH2CH3或CH3COOCH3、CH3COCH2OH(写结构简式).
如图是一种分子式为C3H6O2的有机物的红外光谱谱图,则该有机物的结构简式为:CH3COOCH3

(4)经测定,某有机物含碳77.8%、氢7.4%、氧14.8%;又测得此有机物的蒸气对相同条件下同体积的氢气质量比为54:1,求此有机物的分子式.若此有机物苯环上的一溴代物只有二种,试写出它的可能结构简式.
分析 (1)①乙酸乙酯和乙酸钠溶液,分层;
②乙醇和丁醇互溶,但沸点不同;
③溴化钠和单质溴的水溶液,溴不易溶于水,易溶于有机溶剂;
(2)乙醇易溶于水,己烯和己烷都不溶于水,二者密度都比水小,己烯能与酸性高锰酸钾溶液反应,能使溴水褪色,乙酸具有酸性;
(3)在1H-NMR谱上峰的强度之比等于不同位置氢原子数目之比,峰的给出强度为1:1,说明有2种氢原子,氢原子个数之比为1:1,结构简式为CH3COOCH3;
峰的给出强度为3:2:1,说明有3种氢原子,氢原子个数之比为:3:2:1,结构简式为:CH3CH2COOH或HCOOCH2CH3或CH3COCH2OH;
(4)根据相对密度计算有机物的相对分子质量,根据各元素的含量确定有机物中各原子的个数,进而确定有机物分子式;
根据分子式结合有机物的性质判断有机物可能的结构.
解答 解:(1)①乙酸乙酯和乙酸钠溶液,分层,利用分液分离;
②乙醇和丁醇互溶,但沸点不同,利用蒸馏分离;
③溴化钠和单质溴的水溶液,溴不易溶于水,易溶于有机溶剂,则选择萃取分离,
故答案为:③;
(2)溴水和己烷不反应,混合后分层,溴水可以和己烯发生加成反应使溴水褪色,甲苯、溴乙烷与溴水萃取现象不同,乙酸可利用石蕊鉴别,能鉴别,且较简单,
故答案为:C;
(3)在1H-NMR谱上峰的强度之比等于不同位置氢原子数目之比,峰的给出强度为1:1,说明有2种氢原子,氢原子个数之比为1:1,结构简式为CH3COOCH3;
峰的给出强度为3:2:1,说明有3种氢原子,氢原子个数之比为:3:2:1,结构简式为:CH3CH2COOH或HCOOCH2CH3或CH3COCH2OH;
图是一种分子式为C3H6O2的有机物的红外光谱谱图,含不对称甲基,含-COOC-,则该有机物的结构简式为CH3COOCH3,
故答案为:CH3COOCH3、HCOOCH2CH3或CH3COOCH3、HCOOCH2CH3或CH3COOCH3、CH3COCH2OH;CH3COOCH3;
(4)M(有机物)=54×M(H2)=54×2=108,则有:
N(C)=$\frac{108×77.8%}{12}$=7,
N(H)=$\frac{108×7.4%}{1}$=8,
N(O)=$\frac{108×(1-77.8%-7.4%)}{16}$=1
所以该有机物的分子式为C7H8O,
因该有机物能与烧碱反应,所以是酚.又因苯环上的一溴代物只有二种,
所以其结构简式为: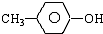 ;
;
答:该有机物的分子式为C7H8O,结构简式为 .
.
点评 本题考查有机物的推断及混合物分离提纯,为高频考点,把握有机物的结构、官能团及分子式确定为解答的关键,侧重分析与推断能力的考查,题目难度不大.

 习题精选系列答案
习题精选系列答案| A. | 该有机物的最简式为 CH3O | B. | 该有机物的分子式可能为 CH3O | ||
| C. | 该有机物的分子式可能为 C2H6O | D. | 该有机物1H核磁共振谱中有两个峰 |
| A. | 淀粉、纤维素、蛋白质都是天然高分子化合物 | |
| B. | 用于奥运“祥云”火炬的丙烷是一种清洁燃料 | |
| C. | 医疗上使用75%的酒精用于消毒 | |
| D. | 糖类、油脂、蛋白质在一定条件下都可发生水解反应 |
| A. | 甲醚作燃料会产生氮的氧化物和碳氢化合物等污染物 | |
| B. | 甲醚可由甲醇在一定条件下发生消去反应而制得 | |
| C. | 甲醚与乙醇是同分异构体 | |
| D. | 1 mol甲醚完全燃烧消耗的氧气与1 mol甲醇完全燃烧消耗的氧气相同 |
| A. | 原子序数X>Y>Z | |
| B. | 元素的非金属性由强至弱的顺序是X>Y>Z | |
| C. | 原子半径大小顺序是X>Y>Z | |
| D. | 气态氢化物的稳定性H3X>H2Y>HZ |
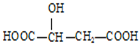 ,下列说法正确的是( )
,下列说法正确的是( )| A. | HOOC-CH2-CH(OH)-COOH与苹果酸互为同分异构体 | |
| B. | 1mol苹果酸可与3mol NaOH发生中和反应 | |
| C. | 1mol苹果酸与足量金属Na反应生成生成1mol H2 | |
| D. | 苹果酸中能发生酯化反应的官能团有2种 |