题目内容
溶液中含有NO3-、SO32-、Cl-和NH4+,若向其中加入足量的盐酸,溶液里上述四种离子浓度基本不变的是 .
考点:离子共存问题
专题:
分析:氯化氢能够电离出氢离子和氯离子,能够与氢离子或氯离子反应的离子的浓度会发生变化,另外加入盐酸后氢离子和氯离子浓度变化较大,据此进行判断.
解答:
解:溶液中含有NO3-、SO32-、Cl-和NH4+,若向其中加入足量的盐酸,SO32-与氢离子反应,浓度变化较大;加入盐酸后溶液中氯离子浓度增大,
所以加入盐酸后溶液中离子浓度变化基本不变的为:NO3-、NH4+,
故答案为:NO3-、NH4+.
所以加入盐酸后溶液中离子浓度变化基本不变的为:NO3-、NH4+,
故答案为:NO3-、NH4+.
点评:本题考查了离子共存,题目难度不大,试题侧重基础知识的考查,明确离子反应发生条件即可解答,本题中加入盐酸后溶液中氯离子浓度变化较大,为易错点.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
下列对于某些离子的检验及结论正确的是( )
| A、某溶液中加入稀盐酸产生无色气体,将产生的气体通入澄清石灰水,石灰水变浑浊,则该溶液中一定含有CO32一 |
| B、某溶液中加入氢氧化钠溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝,则该溶液中一定含有NH4+ |
| C、某溶液中滴入BaCl2溶液,再滴加稀盐酸,产生白色沉淀,则一定含有SO42一 |
| D、某溶液加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,则一定含有Ba2+ |
下列各组物质中,是同系物的是( )
| A、乙烷和己烷 |
| B、CH3COOH、C3H6O2 |
C、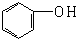 和 和  |
| D、HCHO、CH3COOH |
近期,十一届全国人大常委会第四次会议正式对《食品安全法(草案)》进行了二审,表明国家对食品安全问题越来越重视.工商人士提醒消费者,长期食用二氧化硫含量超标的食品不仅会破坏维生素B1,还会影响人体对钙的吸收.下列说法中一定错误的是( )
| A、二氧化硫遇水生成亚硫酸,容易引起胃肠道反应 |
| B、二氧化硫引起的环境问题主要是酸雨 |
| C、人体直接吸入二氧化硫易引起呼吸道疾病 |
| D、可通过服入碱性物质(如NaOH)的方法来消除二氧化硫中毒 |
在A、B两烧杯溶液中,含有Fe2+、Na+、H+、NO3-、Cl-、OH-6种离子.已知B烧杯的溶液无色(含有其中三种离子),则A烧杯的溶液中大量存在的离子是( )
| A、NO3-、OH-、Cl- |
| B、Fe2+、H+、Cl- |
| C、Fe2+、OH-、NO3- |
| D、Na+、H+、OH- |
25℃时,在等体积的①pH=0的 H2SO4溶液、②0.05mol/L的Ba(OH)2溶液中,发生电离的水的物质的量之比是( )
| A、1:10 | B、1:5 |
| C、1:20 | D、10:1 |
将0.05molBa(OH)2固体分别加入500mL下列液体中,溶液的导电能力变化最小的是( )
| A、自来水 |
| B、0.1mol?L-1的硫酸 |
| C、0.2mol?L-1的醋酸 |
| D、0.2mol?L-1的Na2CO3溶液 |
如图 图片显示的是生锈的铁桥,有关钢铁生锈说法不正确的是( )


| A、铁桥生锈是电化学腐蚀 |
| B、建在海边的铁桥更易生锈 |
| C、钢铁生锈的负极反应是:Fe-3e-=Fe3+ |
| D、吸氧腐蚀的正极反应是:O2+4e-+2H2O=4OH- |
下列实验对应的离子方程式正确的是( )
| A、铝溶解在NaOH溶液中:2Al+2OH-=2AlO2-+3H2↑ |
| B、醋酸溶液滴入NaHCO3溶液中:H++HCO3-=CO2↑+H2O |
| C、SO2通入溴水中:SO2+Br2+H2O=SO42-+2Br-+2H+ |
| D、少量铁溶于过量稀硝酸中:Fe+4H++NO3-=Fe3++NO↑+2H2O |