��Ŀ����
��11�֣�ij�о���ѧϰС������ȷ�Ӧʵ��չ���о������и��л�ѧ�̲ģ�����ѡ�ޣ��жԡ����ȷ�Ӧ��������������������������Ӧ�ų��������ȣ�������ҫ�۵Ĺ�â������ֽ©�����²����մ���������������ɳ�С������ġ���ѧ�ֲᡷ֪��Al��Al2O3��Fe��Fe2O3�۵㡢�е��������£�
���� | Al | Al2O3 | Fe | Fe2O3 |
�۵�/�� | 660 | 2054 | 1535 | 1462 |
�е�/�� | 2467 | 2980 | 2750 | - |
I.��1��ijͬѧ�Ʋ⣬���ȷ�Ӧ���õ���������Ӧ�������Ͻ������ǣ��÷�Ӧ�ų�������ʹ���ۻ����������۵�����ͣ���ʱҺ̬���������ۺ��γ������Ͻ�����Ϊ���Ľ����Ƿ��������_________________(�������������)
��2�����һ����ʵ�鷽����֤���������õĿ�״�������к��н���������ʵ�������Լ���______________,��Ӧ�����ӷ���ʽΪ_________________________________��
��3��ʵ�����ܽ������������Լ�����õ���____________(�����)��
A��Ũ���� B��ϡ����C��ϡ���� D������������Һ
II��ʵ���о����֣����ᷢ��������ԭ��Ӧʱ�������Ũ��Խϡ����Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�͡�ijͬѧȡһ������������������һ������ϡ�������ַ�Ӧ����Ӧ������������ų����ڷ�Ӧ���������Һ�У���μ���4mol��L����������������Һ����������������Һ�����(mL)������ij��������ʵ���(mol)�Ĺ�ϵ��ͼ��ʾ��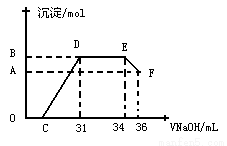 �Իش��������⣺
�Իش��������⣺
��1��ͼ��OC��û�г������ɣ��˽η�����Ӧ�����ӷ���ʽΪ________________��
��2����DE�Σ����������ʵ���û�б仯����˽η�����Ӧ�����ӷ���ʽ_______________ ��
��������˵����Һ��_________________���OH����������_______ǿ�������ӷ��ţ���
��3�� B��A�IJ�ֵΪ_________mol��B���Ӧ�ij��������ʵ���Ϊ________mol��C���Ӧ������������Һ�����Ϊ___________mL
I����1��������2��NaOH��Һ��2Al+2OH-+2H2O=2AlO2-+3H2������3��B��
II����1��H++OH-=H2O����2��NH4++OH-=NH3��H2O��Al3+��Fe3+��H+��NH4+ ����3��0.008��0.032mol��7ml��
��������
���������I����1�� �÷�Ӧ�ų�������ʹ���ۻ����������۵�����ͣ���ʱ��Ӧ������Һ̬�������������ۺ��γ������Ͻ��������Ľ����Ǻ����ģ���2������Al�ܹ���ǿ����Һ������Ӧ������������Fe��Al���ܷ�����Ӧ�����ʼ�����֤�����Ը�ʵ�������Լ���NaOH��Һ����Ӧ�Ļ�ѧ����ʽ�ǣ�2Al+2OH-+2H2O=2AlO2-+3H2�� ����3��A���ڳ����£�Fe��Al��Ũ����ᷢ���ۻ������ܼ���������Ӧ�����Բ�����ʵ�����ܽ�����������B��Fe��Al������ϡ���ᷢ����Ӧ�������������ʼ����������Կ��������ܽ�����ʣ���ȷ�� C��ϡ���������Fe��Al������Ӧ�����ǻ����NO�ȴ�����Ⱦ�����������˲�������ʵ�����ܽ�����������D������������Һֻ����Al��Ӧ��������Fe��Ӧ�����Բ��������ܽ�û�������II����1�����������ܽ�ý�������Һ�м���NaOH��Һ������������������������������NaOH������������ᷢ���кͷ�Ӧ������OC�����ӷ���ʽ�ǣ�H++OH-=H2O����2����CD����Һ�е�Fe3+��Al3+����������Ӧ�γ�Fe(OH)3��Al(OH)3��������DE�Σ����������ʵ���û�б仯������Ϊ��DE��NaOH��Һ�����ᱻ��ԭΪNH4NO3,���߷������ֽⷴӦ�����ӷ���ʽ�ǣ�NH4++ OH-=NH3��H2O����������˵����Һ��Al3+��Fe3+��H+�����OH����������NH4+ǿ����3����EF��NaOH�ܽ�Al(OH)3���������ӷ���ʽ�ǣ�Al(OH)3+ OH-= AlO2-+ 2H2O���ܽ�Al(OH)3���ĵ�NaOH�����ʵ�����n(NaOH)= 4mol/L��0.002L=0.008mol,���Ը��ݷ�Ӧ����ʽ�ж��ߵ����ʵ�����ϵ��֪��n(Al(OH)3)=0.008mol������Al(OH)3�������ĵ�NaOH��Һ�������6ml�����ݷ�Ӧ����ʽNH4++ OH-=NH3��H2O ��֪��n(NH4+)=4mol/L��0.003L=0.012mol��n(e-)=0.012mol��8=0.096mol,Fe��Al����+3�۵Ľ����������ڷ�Ӧ�����е���ת����Ŀ��ȣ�����n(Fe)+n(Al)= 0.096mol��3=0.032mol,������B���Ӧ�ij��������ʵ�������������ʵ�����ȣ�Ϊ0.032mol;ʹAl3+��Fe3+�γɳ������ĵ�NaOH�����ʵ�������ӵ����ʵ�����ȣ���0.096mol ����������NaOH��Һ�������V��NaOH��=0.096mol ��4mol/L=0.024L=24ml,���� C���Ӧ������������Һ�����Ϊ31ml-24ml=7ml��
���㣺�����غ㷨�ڻ�����и��ɷֵ�ȷ����Ӧ�õ�֪ʶ��

 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д�

 D����ά�ص�ͨʽ��(C6H12O6)n
D����ά�ص�ͨʽ��(C6H12O6)n ��
��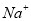 ��
��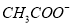 ��Br-
��Br- 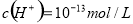 ����Һ��
����Һ��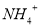 ��
��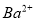 ��
��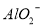 ��
��