题目内容
氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40-50℃时反应可生成它.CuH不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生反应是2Cu+═Cu2++Cu.根据以上信息,结合自己所掌握的化学知识,回答:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是 .
(2)写出CuH在氯气中燃烧的化学反应方程式 .
(3)CuH溶解在稀硫酸中生成的气体是 ,如果反应中生成了标况下22.4L的气体,转移电子的物质的量是 .
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是
(2)写出CuH在氯气中燃烧的化学反应方程式
(3)CuH溶解在稀硫酸中生成的气体是
考点:铜金属及其重要化合物的主要性质
专题:几种重要的金属及其化合物
分析:(1)根据化合价的变化判断氧化剂、还原剂;
(2)CuH在氯气中燃烧,氯气做氧化剂,CuH做还原剂;
(3)CuH溶解在稀盐酸中,CuH中的H-失电子,盐酸中H+得电子,据此分析计算即可.
(2)CuH在氯气中燃烧,氯气做氧化剂,CuH做还原剂;
(3)CuH溶解在稀盐酸中,CuH中的H-失电子,盐酸中H+得电子,据此分析计算即可.
解答:
解:(1)根据化合价的变化判断,CuSO4做氧化剂、所以另一物质做还原剂,故答案为:还原剂;
(2)CuH在氯气中燃烧,氯气做氧化剂,CuH做还原剂,所以反应方程式为:2CuH+3Cl2
2CuCl2+2HCl,故答案为:2CuH+3Cl2
2CuCl2+2HCl;
(3)CuH溶解在稀盐酸中,CuH中的H-失电子,盐酸中H+得电子,所以得到的气体是H2;在此反应中CuH中Cu的化合价由+1价升高到+2价,H的化合价由-1价升高到0价,故反应方程式为:2CuH+2H2SO4=2CuSO4+3H2↑,已知生成气体的物质的量为
=1mol,故依据方程式得出转移电子数为1.5mol,故答案为:H2;1.5mol.
(2)CuH在氯气中燃烧,氯气做氧化剂,CuH做还原剂,所以反应方程式为:2CuH+3Cl2
| ||
| ||
(3)CuH溶解在稀盐酸中,CuH中的H-失电子,盐酸中H+得电子,所以得到的气体是H2;在此反应中CuH中Cu的化合价由+1价升高到+2价,H的化合价由-1价升高到0价,故反应方程式为:2CuH+2H2SO4=2CuSO4+3H2↑,已知生成气体的物质的量为
| 22.4L |
| 22.4L/mol |
点评:本题是信息给予题,筛选有用信息结合已学知识进行整合处理.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
下列实验过程中产生的变化与对应的图形相符合的是( )
A、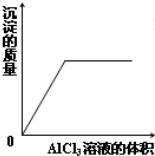 AlCl3溶液滴入NaOH溶液中 |
B、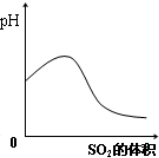 SO2气体通入氢硫酸中 |
C、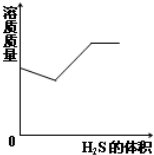 H2S气体通入NaOH溶液中 |
D、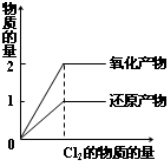 在一定量的H2S水溶液中逐渐通入Cl2 |