题目内容
在硫酸钠和硫酸钾的混和溶液中,当n(Na+)=0.2mol,n(SO42-)=x mol,n(K+)=y mol时,则x和y的关系是( )
| A、y=2(x+0.1) | ||
B、x=
| ||
| C、y=2x-0.1 | ||
D、x=0.1+
|
考点:物质的量的相关计算
专题:守恒思想
分析:根据溶液中阴阳离子所带的正负电荷总数相等,则有c(Na+)+c(K+)=2c(SO42-),据此计算.
解答:
解:根据溶液中阴阳离子所带的正负电荷总数相等,则有c(Na+)+c(K+)=2c(SO42-),在硫酸钠和硫酸钾的混和溶液中,体积相同,假设体积为1升,即:
0.2mol/L×1+ymol/L×1=xmol/L×2,解得:x=0.1+
,
故选D.
0.2mol/L×1+ymol/L×1=xmol/L×2,解得:x=0.1+
| y |
| 2 |
故选D.
点评:本题主要考查溶液物质的量的计算,题目难度不大,注意电荷守恒原则在混合溶液有关离子浓度计算运用.

练习册系列答案
相关题目
比较乙烷和乙醇的结构,下列说法错误的是( )
| A、两个碳原子以单键相连 |
| B、乙基与一个氢原子相连就是乙烷分子 |
| C、分子里都含6个相同的氢原子 |
| D、乙基与一个羟基相连就是乙醇分子 |
 镁_次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主 要工作原理如右图所示,其正极反应为:ClO-+H2O+2e-═Cl-+2OH-,关于该电池的叙述正确的是( )
镁_次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主 要工作原理如右图所示,其正极反应为:ClO-+H2O+2e-═Cl-+2OH-,关于该电池的叙述正确的是( )| A、该电池中镁为负极,发生还原反应 |
| B、电池工作时,OH-向正极移动 |
| C、电池工作时,正极周围溶液的pH将不断变小 |
| D、该电池的总反应式为:Mg+ClO-+H2O═Mg(OH)2↓+Cl- |
分子式为C4H8O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些醇和酸重新组合可形成的酯共有( )
| A、1种 | B、5种 | C、9种 | D、12种 |
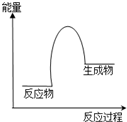 根据如图提供的信息,不能够得到的结论是( )
根据如图提供的信息,不能够得到的结论是( )| A、该反应一定有能量转化成了生成物的化学能 |
| B、该反应中化学能转化成了热能,为放热反应 |
| C、该反应生成物的总能量高于反应物的总能量 |
| D、该反应过程中有比生成物能量更高的中间物质生成 |
有人建议将氢排在周期表的ⅦA族,能支持这一观点的是( )
①氢原子得一个电子实现最外电子层稳定结构;
②氢气分子中氢原子间的化学键是共价键;
③氢元素与碱金属元素可形成离子化合物M+[:H]-.
①氢原子得一个电子实现最外电子层稳定结构;
②氢气分子中氢原子间的化学键是共价键;
③氢元素与碱金属元素可形成离子化合物M+[:H]-.
| A、①② | B、①③ | C、②③ | D、①②③ |
湿法脱硝技术可用于处理烟气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g)
2N2(g)+3H2O(g)△H<0
在恒容的密闭容器中,按2:1:1的比例通入NH3、NO、NO2混合气体,平衡时氮氧化物去除率可达80%.下列有关说法正确的是( )
2NH3(g)+NO(g)+NO2(g)
| 180℃ |
| 催化剂 |
在恒容的密闭容器中,按2:1:1的比例通入NH3、NO、NO2混合气体,平衡时氮氧化物去除率可达80%.下列有关说法正确的是( )
| A、若其他条件不变,反应温度改为400℃,能更快达到同样的氮氧化物去除率 |
| B、若其他条件不变,改用高效催化剂,能更快达到同样的氮氧化物去除率 |
| C、平衡时,其他条件不变,再向容器中通入NH3,氮氧化物去除率将高于80% |
| D、平衡时,其他条件不变,再升高温度可使该反应的平衡常数增大 |
下列叙述正确的是( )
| A、SO3的水溶液能导电,所以SO3是电解质 |
| B、氯化钠晶体不导电,但是氯化钠是电解质 |
| C、氯化钠溶液能导电,所以氯化钠溶液是电解质 |
| D、液态氯化氢不能导电,但是氯化氢是电解质 |
对于10%H2O2的分解反应,下列措施能减缓其化学反应速率的是( )
| A、加入MnO2 |
| B、加水稀释 |
| C、加热 |
| D、加入30%的H2O2 |