题目内容
6.书写下列物质在水溶液中的电离方程式:KCl=K++Cl-
Na2SO4=2Na++SO42-
BaCl2=Ba2++2Cl-
NaHSO4=Na++H++SO42-
NaHCO3=Na++HCO3-.
分析 明确电解质的强弱,强电解质完全电离,用等号,弱电解质部分电离,用可逆号,注意电离方程式书写遵循原子个数、电荷守恒规律.
解答 解:氯化钾为强电解质,完全电离,电离方程式:KCl=K++Cl-;
故答案为:KCl=K++Cl-;
硫酸钠为强电解质,完全电离,电离方程式:Na2SO4=2Na++SO42-;
故答案为:Na2SO4=2Na++SO42-;
氯化钡为强电解质,完全电离,电离方程式:BaCl2=Ba2++2Cl-;
故答案为:BaCl2=Ba2++2Cl-;
硫酸氢钠强电解质,水溶液中完全电离出钠离子、氢离子、硫酸根离子,电离方程式:NaHSO4=Na++H++SO42-;
故答案为:NaHSO4=Na++H++SO42-;
碳酸氢钠强电解质,水溶液中完全电离出钠离子、碳酸氢根离子,电离方程式:NaHCO3=Na++HCO3-;
故答案为:NaHCO3=Na++HCO3-.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱及电离方式是解题关键,注意碳酸氢根为弱酸的酸式根离子,不能拆,题目难度不大.

练习册系列答案
相关题目
16.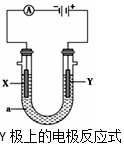 电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:
电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:
(1)若X、Y都是惰性电极,a是硫酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,一段时间后,在X极附近观察到的现象是溶液变蓝、产生气泡,Y极上的电极反应式为4OH--4e-=2H2O+O2↑.
(2)若X、Y都是惰性电极,a是CuSO4溶液,电解一段时间后,阳极上产生气体的体积为0.224L(标准状况下),则阴极上析出金属的质量为1.28g;
(3)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是D (填序号).
 电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:
电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:(1)若X、Y都是惰性电极,a是硫酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,一段时间后,在X极附近观察到的现象是溶液变蓝、产生气泡,Y极上的电极反应式为4OH--4e-=2H2O+O2↑.
(2)若X、Y都是惰性电极,a是CuSO4溶液,电解一段时间后,阳极上产生气体的体积为0.224L(标准状况下),则阴极上析出金属的质量为1.28g;
(3)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是D (填序号).
| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | Fe(NO3)3 |
| D | 铁 | 银 | AgNO3 |
17.在某无色透明的酸性溶液中,能共存的离子组是( )
| A. | Na+、K+、SO4 2-、HCO3 - | B. | Cu2+、K+、SO4 2-、NO3- | ||
| C. | Na+、K+、Cl-、NO3- | D. | Fe3+、K+、SO4 2-、Cl - |
1.遇到下列情况时,其处理方法有误的是( )
| A. | 将CO中毒者转移到通风处抢救 | |
| B. | 皮肤上不慎沾有浓碱液,立即用大量水冲洗,然后涂上2% 的硼酸溶液 | |
| C. | 少量酒精失火时,立即用湿抹布盖灭 | |
| D. | 夜间进入厨房,闻到很浓的煤气味,立即开灯检查 |
11.T℃时.体积均为0.5L的两个恒容密闭容器中发生可逆反应:2A(g)+B(g)?2C(g)△H=-Q kJ/mol(Q>0)实验测得反应在起始、达到平衡时的有关数据如表,下列叙述正确的是( )
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡时体系能量的变化 | ||
| A | B | C | ||
| ① | 2 | 1 | 0 | 0.75 Q kJ |
| ② | 0.4 | 0.2 | 1.6 | |
| A. | 容器①、②中的平衡常数均为36 | |
| B. | 向容器①中通入氦气,平衡时A的转化率不变 | |
| C. | 容器②中达到平衡时放出的热量为0.05 Q kJ,达到平衡时,两个容器中C的物质的量浓度均为1.5 mol•L-1 | |
| D. | 其他条件不变,若容器②保持恒容绝热,则达到平衡时C的体积分数小于2/3 |
15.下列说法不正确的是( )
| A. | 氧化还原反应的特征是元素化合价发生了变化 | |
| B. | 在水溶液中能电离出H+的化合物不一定是酸 | |
| C. | 在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定不相同 | |
| D. | 因为NH3溶于水的溶液能导电,所以NH3是电解质 |