题目内容
某混合物A中含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下列所示的物质之间的转变[已知:NaAlO2+CO2+2H2O═Al(OH)3↓+NaHCO3]:

据此判断:
(1)固体B所含物质的化学式为 .
(2)固体E所含物质的化学式为 、 .
(3)有人认为,过量氨水可以用过量NaOH溶液代替,你认为正确吗?为什么? .
(4)第一次沉淀加入NaOH溶液后的离子方程式为 .
(5)反应①的离子方程式为 .

据此判断:
(1)固体B所含物质的化学式为
(2)固体E所含物质的化学式为
(3)有人认为,过量氨水可以用过量NaOH溶液代替,你认为正确吗?为什么?
(4)第一次沉淀加入NaOH溶液后的离子方程式为
(5)反应①的离子方程式为
考点:无机物的推断,物质的检验和鉴别的实验方案设计
专题:实验设计题
分析:KAl(SO4)2溶于水,Al2O3和Fe2O3均不溶于水,混合物A加水溶解后,溶液中是KAl(SO4)2,沉淀是Al2O3和Fe2O3;
向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,Al(OH)3受热分解生成Al2O3;
向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中剩余的是K2SO4 和(NH4)2SO4,经过蒸发、结晶,得到的是K2SO4 和(NH4)2SO4;
向NaAlO2溶液中通入过量CO2可得Al(OH)3沉淀和碳酸氢钠,以此来解答.
向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,Al(OH)3受热分解生成Al2O3;
向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中剩余的是K2SO4 和(NH4)2SO4,经过蒸发、结晶,得到的是K2SO4 和(NH4)2SO4;
向NaAlO2溶液中通入过量CO2可得Al(OH)3沉淀和碳酸氢钠,以此来解答.
解答:
解:KAl(SO4)2溶于水,Al2O3和Fe2O3均不溶于水,混合物A加水溶解后,溶液中是KAl(SO4)2,沉淀是Al2O3和Fe2O3;
向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,Al(OH)3受热分解生成固体B为Al2O3;
向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中剩余的是K2SO4 和(NH4)2SO4,经过蒸发、结晶,得到的固体E为K2SO4 和(NH4)2SO4;
向NaAlO2溶液中通入过量CO2可得Al(OH)3沉淀和碳酸氢钠,
(1)由上述分析可知,B为Al2O3,故答案为:Al2O3;
(2)由上述分析可知,E中含(NH4)2SO4、K2SO4,故答案为:(NH4)2SO4;K2SO4;
(3)因氢氧化铝具有两性,NaOH会把Al3+全部转化为为Al02-,而无法得到Al(OH)3沉淀,则做法不正确,故答案为:不正确;NaOH会把Al3+全部转化为Al02-,而无法得到Al(OH)3沉淀;
(4)第一次沉淀加入NaOH溶液后,只有氧化铝与碱反应,其离子方程式为Al2O3+2OH-═2AlO2-+H2O,故答案为:Al2O3+2OH-═2AlO2-+H2O;
(5)反应①中二氧化碳过量,反应生成沉淀和碳酸氢钠,其离子方程式为AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,故答案为:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-.
向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,Al(OH)3受热分解生成固体B为Al2O3;
向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中剩余的是K2SO4 和(NH4)2SO4,经过蒸发、结晶,得到的固体E为K2SO4 和(NH4)2SO4;
向NaAlO2溶液中通入过量CO2可得Al(OH)3沉淀和碳酸氢钠,
(1)由上述分析可知,B为Al2O3,故答案为:Al2O3;
(2)由上述分析可知,E中含(NH4)2SO4、K2SO4,故答案为:(NH4)2SO4;K2SO4;
(3)因氢氧化铝具有两性,NaOH会把Al3+全部转化为为Al02-,而无法得到Al(OH)3沉淀,则做法不正确,故答案为:不正确;NaOH会把Al3+全部转化为Al02-,而无法得到Al(OH)3沉淀;
(4)第一次沉淀加入NaOH溶液后,只有氧化铝与碱反应,其离子方程式为Al2O3+2OH-═2AlO2-+H2O,故答案为:Al2O3+2OH-═2AlO2-+H2O;
(5)反应①中二氧化碳过量,反应生成沉淀和碳酸氢钠,其离子方程式为AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,故答案为:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-.
点评:本题考查无机物的推断,为高频考点,把握物质的性质及框图中发生的化学反应为解答的关键,侧重分析与推断能力的考查,题目难度不大.

练习册系列答案
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
下列说法正确的是( )
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
②物质的溶解度随温度的升高而增加,物质的溶解都是吸热的;
③对于Al(OH)3(s)?Al(OH)3(aq)?Al3++3OH-,前者为溶解平衡,后者为电离平衡;
④除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3小;
⑤沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全.
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
②物质的溶解度随温度的升高而增加,物质的溶解都是吸热的;
③对于Al(OH)3(s)?Al(OH)3(aq)?Al3++3OH-,前者为溶解平衡,后者为电离平衡;
④除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3小;
⑤沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全.
| A、①②③④⑤ | B、② |
| C、①③④⑤ | D、①②⑤ |
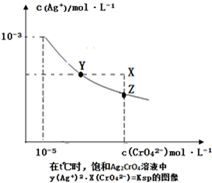 已知t℃时AgCl的Ksp=4×10-l0,在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是( )
已知t℃时AgCl的Ksp=4×10-l0,在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是( )| A、在t℃时,Ag2CrO4的Ksp为1×10-11 |
| B、在饱和溶液中加入K2CrO4可使溶液由Y点到Z点 |
| C、在t℃时,Ag2CrO4(s)+2Cl-(aq)?2AgCl(s)+CrO42-(aq)平衡常数K=6.25×107 |
| D、在t℃时,以0.001mol/L AgNO3溶液滴定20mL 0.001mol/L KCl和0.001mol/L的K2CrO4的混和溶液,CrO42-先沉淀 |
某混合气体是由HF、(HF)2、(HF)3三种气体组成,该混合气体的平均相对分子质量为38,则混合气体中HF的体积分数为( )
| A、大于10% | B、小于10% |
| C、等于10% | D、无法计算 |
将1L含有0.4molCuSO4和0.1molNaCl的水溶液用惰性电极电解,电解一段时间后,在一个电极上得到0.25molCu,另一个电极上产生气体(标况)的体积是( )
| A、4.48L |
| B、3.36L |
| C、6.72L |
| D、13.44L |
在盛有碘水的试管中,加入少量CCl4后振荡,静置片刻后( )
| A、上层为无色,下层为紫红色 |
| B、整个溶液变为棕黄色 |
| C、整个溶液变紫色 |
| D、下层无色,上层紫红色 |
化学与生活密切相关,下列说法不正确的是( )
| A、“地沟油”禁止食用,但可以用来制肥皂 |
| B、PM 2.5作为空气质量预报的一项重要指标,它是指空气中直径小于或等于2.5um的颗粒物,该值越高,代表空气污染程度越严重 |
| C、积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料 |
| D、碳酸钡是一种难溶于水和酸的盐,可用作X光透视肠胃的药剂 |
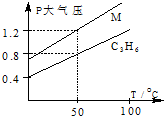 如图中两条曲线分别表示1g C3H6、1g M气体在相同体积的容器中压强和温度的关系,试根据图判断M气体可能是( )
如图中两条曲线分别表示1g C3H6、1g M气体在相同体积的容器中压强和温度的关系,试根据图判断M气体可能是( )| A、C3H4 |
| B、CO2 |
| C、CO |
| D、H2S |