题目内容
16.已知可逆反应:N(g)+M(g)?P(g)+Q(g)△H>0,请回答下列问题:(1)若要增大M的转化率,在其他条件不变的情况下可以采取的措施为BC(填字母).
A.加入一定量M B.加入一定量N
| 温度/℃ | 600 | 700 |
| 平衡常数 | K1 | K2 |
D.缩小反应容器的体积
(2)不同温度下该反应的平衡常数如下:则K1< (填“>”或“<”)K2.
(3)某温度下,反应物的起始浓度[M]=1.0mol•L-1,[N]=2.4mol•L-1,达到平衡后,M的转化率为60%,此时N的转化率为25%,该反应的平衡常数Kc=0.5.
分析 (1)若要增大M的转化率,需要平衡正向进行,两种反应物增加一种会提高另一种物质的转化率,结合平衡移动原理分析选项;
(2)反应是吸热反应,升温平衡正向进行,平衡常数增大;
(3)依据平衡三行计算列式计算,
N(g)+M(g)?P(g)+Q(g)
起始量(mol/L) 2.4 1.0 0 0
变化量(mol/L) 0.6 0.6 0.6 0.6
平衡量(mol/L) 1.8 0.4 0.6 0.6
转化率=$\frac{消耗量}{起始量}$×100%,
平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$.
解答 解:(1)N(g)+M(g)?P(g)+Q(g)△H>0,反应是气体体积不变的吸热反应,
A.加入一定量M平衡正向进行,但M的转化率减小,故A错误;
B.加入一定量N会提高M的转化率,故B正确;
C.将生成的气体P液化分离,平衡正向进行,可以提高M的转化率,故C正确;
D.缩小反应容器的体积,体系压强增大,反应前后气体体积不变,平衡不变,故D错误;
故答案为:BC;
(2)N(g)+M(g)?P(g)+Q(g)△H>0,反应是气体体积不变的吸热反应,升温平衡正向进行,平衡常数增大,则K1<K2,
故答案为:<;
(3)依据平衡三行计算列式计算,
N(g)+M(g)?P(g)+Q(g)
起始量(mol/L) 2.4 1.0 0 0
变化量(mol/L) 0.6 0.6 0.6 0.6
平衡量(mol/L) 1.8 0.4 0.6 0.6
N的转化率=$\frac{消耗量}{起始量}$×100%=$\frac{0.6mol/L}{2.4mol/L}$×100%=25%,
平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$=$\frac{0.6×0.6}{1.8×0.4}$=0.5,
故答案为:25%,0.5.
点评 本题考查了影响化学平衡的因素、平衡常数随温度变化、平衡计算应用,掌握基础是解题关键,题目较简单.

 备战中考寒假系列答案
备战中考寒假系列答案| A. | 元素的化学性质随着相对原子质量的递增而呈周期性变化 | |
| B. | 元素的最外层电子数等于元素的最高化合价 | |
| C. | 原子序数越大,原子半径越大 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
| A. | 标准状况下,2.24LCHCl3中含有碳氯键数目为0.3NA | |
| B. | 25℃时,0.1mol/L的Na2CO3溶液中含有Na+的数目为0.02NA | |
| C. | 28gN2和CO的混合气体中含有的分子数为NA | |
| D. | 1molNa2O和1molNa2O2的混合物中,含有的离子总数为7NA |
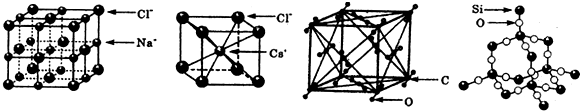
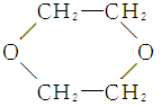
下列关于这些晶体结构和性质的叙述不正确的是( )
| A. | 干冰的晶胞中含有6个CO2分子 | |
| B. | 干冰是分子晶体,其中不仅存在分子间作用力,而且也存在共价键 | |
| C. | 在二氧化硅晶体中,平均每个Si原子形成4个Si-O共价单键 | |
| D. | 同一主族的元素与另一相同元素所形成的化学式相似的物质不一定具有相同的晶体结构 |

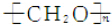
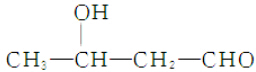
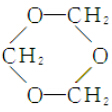
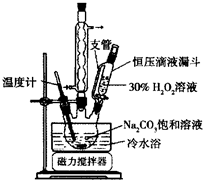 2Na2CO3•3H2O2是一种新型的氧系漂白剂.某实验兴趣小组进行了如下实验.
2Na2CO3•3H2O2是一种新型的氧系漂白剂.某实验兴趣小组进行了如下实验.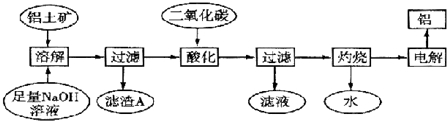
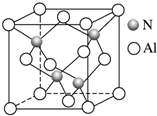 某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域.
某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域.