题目内容
同质量的锌与稀硫酸反应产生氢气,欲使反应速率最大,选择下列组合中的反应条件:①锌粒②锌片③锌粉④98%的浓硫酸⑤15%的稀硫酸⑥20%的稀硫酸⑦加热⑧用冰冷却⑨不断搅拌⑩迅速加入锌片后静置( )
| A、②⑥⑦⑩ | B、①④⑧⑩ |
| C、③⑤⑦⑨ | D、③⑥⑦⑨ |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:加快反应速率的因素有增加反应物浓度、升温、加压、加催化剂、增大反应物接触面积等,根据反应速率影响因素解答即可. 锌粉的接触面积比锌片和锌粒大,
解答:
解:解锌粉的接触面积比锌片和锌粒大,反应速率快,选择③;
浓硫酸和锌反应生成二氧化硫气体不能生成氢气,20%的稀硫酸比15%的稀硫酸浓度大,反应速率快,选⑥;
温度升高,反应速率加快,选⑦;
搅拌可以使反应物充分接触,反应速率加快,选⑨;
综上所述,可以选择③⑥⑦⑨,
故选:D.
浓硫酸和锌反应生成二氧化硫气体不能生成氢气,20%的稀硫酸比15%的稀硫酸浓度大,反应速率快,选⑥;
温度升高,反应速率加快,选⑦;
搅拌可以使反应物充分接触,反应速率加快,选⑨;
综上所述,可以选择③⑥⑦⑨,
故选:D.
点评:本题考查了影响化学反应速率的影响,注重了基础知识的考查,本题难度中等,注意浓硫酸和锌反应不能生成氢气而是生成二氧化硫.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
将BaO2放入密闭真空容器中,反应2BaO2(s)?2BaO(s)+O2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡时,下列说法正确的是( )
| A、平衡常数减小 |
| B、BaO量不变 |
| C、氧气浓度增大 |
| D、BaO2量增加 |
下列有机物不是同一种物质的是( )
A、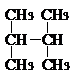 与 与 |
B、 与新戊烷 与新戊烷 |
C、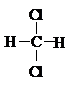 与 与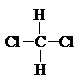 |
| D、C(CH3)3C(CH3)3与CH3(CH2)3C(CH3)3 |
T℃时,A气体与B气体反应生成C气体.反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是( )


| A、在t1min时,3V正(B)=2V逆(C) |
| B、(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动 |
| C、T℃时,在相同容器中,若由0.3mol?L-1A、0.1 mol?L-1 B和0.4 mol?L-1 C反应,达到平衡后,C的浓度仍为0.4 mol?L-1 |
| D、其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
某温度下,反应H2(g)+I2(g) 2HI(g);△H>0.在一带有活塞的密闭容器中达到平衡,下列说法中不正确的是( )
| A、恒温,压缩体积,平衡不移动,混合气体颜色加深 |
| B、恒压,充入HI(g),开始时正反应速率减小 |
| C、恒容,升高温度,逆反应速率减小 |
| D、恒容,充入H2,再次达到平衡时H2(g)的体积分数增大 |
下列物质是非电解质的是( )
| A、CO2 |
| B、AgCl |
| C、Cu |
| D、氨水 |
学校餐厅内长期使用不锈钢餐具,它也不会生锈的原因是在炼钢的过程中加入了下列物质的( )
| A、铬、锰 | B、铬、硅 |
| C、铬、镍 | D、铬、碳 |
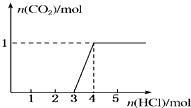 一定量CO2通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(CO2)的关系如图所示.下列有关叙述正确的是( )
一定量CO2通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(CO2)的关系如图所示.下列有关叙述正确的是( )| A、通入的CO2气体在标准状况下等于11.2 L |
| B、溶液中n(NaOH)=2n(Na2CO3) |
| C、A溶液中既含Na2CO3,又含NaHCO3 |
| D、A溶液中一定只有Na2CO3 |