题目内容
9.下列实验设计方案错误的是( )| A. | 除去Cu(NO3)2溶液中混有的AgNO3:加入适量铜粉 | |
| B. | 分离溴和CCl4的混合物:分液 | |
| C. | 区分NaCl和KCl溶液:焰色反应 | |
| D. | 检验某未知溶液中的SO42-:加入稀硝酸酸化的BaCl2溶液 |
分析 A.铜可置换出银;
B.溴易溶于四氯化碳;
C.钠和钾的焰色反应不同;
D.不能排除SO32-的影响.
解答 解:A.加入适量铜粉,可置换出银,同时生成硝酸铜,可用于除杂,故A正确;
B.溴易溶于四氯化碳,二者不分层,应用蒸馏的方法分离,故B错误;
C.钠和钾的焰色反应不同,可用焰色反应鉴别,故C正确;
D.加入硝酸,不能排除SO32-的影响,应先加入盐酸,再加入氯化钡鉴别,故D错误.
故选BD.
点评 本题考查物质的检验、鉴别以及分离、提纯等知识,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,把握实验的严密性和可行性的评价,难度不大.

练习册系列答案
相关题目
19.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 天然气、太阳能、生物质能、风能、氢能均属于新能源 | |
| C. | 自发反应的熵一定增大,非自发反应的熵一定减小 | |
| D. | 常温下,反应C(s)+CO2(g)?2CO(g)不能自发进行,则该反应的△H>0 |
17.将Mg、Cu组成的2.64g混合物投入适量稀硝酸中恰好反应,固体完全溶解时收集到还原产物NO气体0.896L(标准状况),向反应后溶液中加入2mol•L-1NaOH溶液60mL时金属离子恰好沉淀完全.则形成沉淀的物质的量为( )
| A. | 0.03mol | B. | 0.06mol | C. | 0.12mol | D. | 0.24mol |
14.已知1.505×1023个A气体分子的质量为16g,则A气体的摩尔质量是( )
| A. | 64g/mol | B. | 32g/mol | C. | 32g | D. | 16g |
18.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | lmolNacl 固体中含有NA个Na+ | |
| B. | 18gD2O和18gH2 O中含有的质子数均为10NA | |
| C. | 标准状况下2.24LH2O 含有的共价键数为0.2NA | |
| D. | 密闭容答中2molNO 与lmolO2充分反应,产物的分子数为2NA |
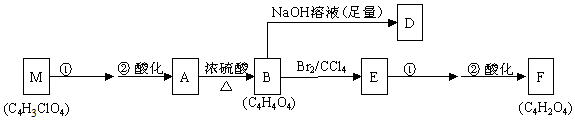
 +(2n-1)H2O .
+(2n-1)H2O . .
.