题目内容
18.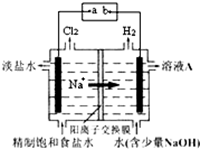 氯碱工业中电解饱和食盐水的原理示意图如图所示.
氯碱工业中电解饱和食盐水的原理示意图如图所示.(1)电极b是电源的负极;
(2)溶液A的溶质是(填化学式)NaOH;
(3)电解饱和食盐水的化学方程式是2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2NaOH.
(4)电解时用盐酸控制阳极区溶液的pH在2~3.用化学平衡移动原理解释盐酸的作用:Cl2与水的反应为Cl2+H2O?HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出.
(5)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mol Cl2参与反应时释放出145kJ热量,写出该反应的热化学方程:2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)△H=-290.0 kJ•mol-1.
分析 (1)依据装置图中氯气和氢气生成的位置判断,生成氯气的电极为阳极,和电源正极相连,生成氢气的电极为阴极,和电源的负极相连;
(2)依据装置图中氯气和氢气生成的位置判断,生成氯气的电极为阳极,a为正极,b为负极,连接电极为阴极,溶液中氢离子在阴极得到电子生成氢气,氢氧根离子浓度增大,溶液A为氢氧化钠溶液;
(3)电解饱和食盐水,依据电极反应判断生成产物,书写离子方程式;
(4)根据阳极产物和平衡移动原理分析;
(5)根据热化学方程式的含义和书写方法来回答.
解答 解:(1)装置图中氯气和氢气生成的位置判断,生成氢气的电极为阴极,和电源负极相连,所以电极b是电源的负极,
故答案为:负极;
(2)装置图中氯气和氢气生成的位置判断,生成氯气的电极为阳极,a为正极,b为负极,连接电极为阴极,溶液中氢离子在阴极得到电子生成氢气,氢氧根离子浓度增大,溶液A为氢氧化钠溶液,
故答案为:NaOH;
(3)电解饱和食盐水,溶液中的氯离子在阳极失电子生成氯气,氢离子在阴极得到电子生成氢气,阴极附近氢氧根离子浓度增大生成氢氧化钠,反应的化学方程式:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2NaOH,
故答案为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2NaOH;
(4)电解时用盐酸控制阳极区溶液的pH在2~3的作用是促使化学平衡Cl2+H2O?HCl+HClO向左移动,减少Cl2在水中的溶解,有利于Cl2的逸出,
故答案为:Cl2与水的反应为Cl2+H2O?HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出;
(5)1molCl2参与反应时释放出145KJ热量,则反应2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)会放出290KJ的能量,即2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)△H=-290.0 kJ•mol-1,
故答案为:2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)△H=-290.0 kJ•mol-1.
点评 本题考查了电解池原理的分析应用,主要是电极反应,电极判断,热化学方程式的书写,题目难度中等.

 阅读快车系列答案
阅读快车系列答案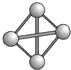 W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.
W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第VIA族;
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式)
(3)W、Y、Z、G形成的简单离子的半径大小顺序是Cl->N3->O2->Na+(用化学符号表示)
(4)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有O3、Cl2、ClO2 (任写两个)
(5)Y与M的氢化物中,热稳定性差的是H2S(填化学式),沸点高的是H2O(填化学式)
(6)ZW的电子式为Na+[:H]-,W2Y2的电子式为
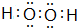 ,用电子式表示Z2M的形成过程:
,用电子式表示Z2M的形成过程: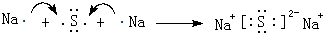 .
.(7)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,品红溶液不褪色(填“褪色”或“不褪色”),请用相关离子方程式解释原因SO2+Cl2+2H2O=SO42-+2Cl-+4H+.
(8)已知
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
(9)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N入出942kJ.根据以上信息和数据,下列说法正确的是C.
A.N4属于一种新型化合物
B.N4晶体熔点高,硬度大
C.相同质量的N4的能量高于N2
D.1molN4转变为N2将吸收882KJ的能量.
| A. | 常温下,由水电离出的c(H+)=10-12mol/L,则溶液pH一定为12 | |
| B. | 已知H2C2O4是弱酸,其电离方程式为:H2C2O4?2H++C2O42- | |
| C. | 常温下,pH=10的氨水溶液中,由水电离出的c(H+)=10-10mol/L | |
| D. | 工业合成氨温度控制在500℃,目的是为了提高产率 |
(1)为了加快反应速率,不可以采取的措施有ABC (填序号,下同).
A.使用催化剂 B.提高氧气的浓度
C.提高反应的温度 D.降低反应的温度
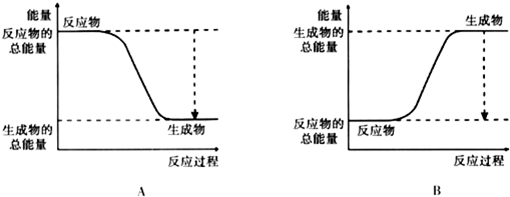
(2)已知该反应为放热反应,如图能正确表示该反应中能量变化的是A
(3)从断键和成键的角度分析上述反应中能量的变化.已知化学键的键能如表:
| 化学键 | H-H | O=O | H-O |
| 键能kJ•mol-1 | 436 | 496 | 463 |
| A. | 石墨 | B. | 氧化铜 | C. | 浓盐酸 | D. | 醋酸钠固体 |
| A. | 氯离子的结构示意图: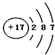 | B. | 18g18O2中含有1mol氧原子 | ||
| C. | 14N和14C是互为同位素 | D. | 氨气的电子式为: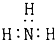 |

