题目内容
3.“8.12”天津港特大爆炸事故中,现场存有大量危险品氰化钠(NaCN),CN-能与人体血红蛋白中的Fe2+结合,因而有剧毒,泄露的氰化钠可通过喷洒双氧水的方式来处理.试回答下列问题:(1)已知CN-中各原子均满足8电子稳定结构,写出其电子式:
 .
.(2)NaCN溶液显碱性,原因是:CN-+H2O?HCN+OH-(用离子方程式表示).
(3)用双氧水处理氰化钠时生成一种常见酸式盐和一种常见的碱性气体,写出该反应的化学反应方程式:NaCN+H2O2+H2O=NaHCO3+NH3.
(4)某废水中CN-浓度为26mg•L-1,用氯气处理1m3该废水将CN-转化为两种无污染气体,理论上至少需要消耗标况下氯气的体积为56L.
分析 (1)NaCN为离子化合物,CN-中各原子均满足8电子稳定结构,存在C≡N键;
(2)NaCN为强碱若酸盐,水解呈碱性;
(3)氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3;
(4)用氯气处理1m3该废水将CN-转化为两种无污染气体,应生成二氧化碳和氮气,结合方程式计算.
解答 解:(1)CN-中各原子均满足8电子稳定结构,存在C≡N键,电子式为 ,故答案为:
,故答案为: ;
;
(2)NaCN为强碱若酸盐,水解呈碱性,离子方程式为CN-+H2O?HCN+OH-,故答案为:CN-+H2O?HCN+OH-;
(3)碱性气体为氨气,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,反应的化学方程式为:NaCN+H2O2+H2O=NaHCO3+NH3,
故答案为:NaCN+H2O2+H2O=NaHCO3+NH3;
(4)反应的方程式为:2KCN+5Cl2+4H2O=2KCl+8HCl+N2+2CO2,废水中CN-浓度为26mg•L-1,1m3该废水中n(CN-)=$\frac{1000L×26mg/L×1{0}^{-3}g/mg}{26g/mol}$=1mol,
则需要2.5mol氯气,体积为2.5mol×22.4L/mol=56L.
故答案为:56.
点评 本题考查氧化还原反应的计算,为高考常见题型和高频考点,侧重于学生的分析能力和计算能力的考查,注意从元素化合价的角度认识氧化还原反应的相关概念和物质的性质,难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
13.下列选项中,表示ⅥA族某元素原子结构示意图的是( )
| A. | 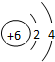 | B. | 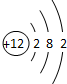 | C. | 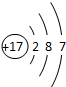 | D. | 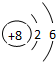 |
14.下列化学用语表述正确的是( )
| A. | 甲烷的球棍模型: | B. | 氯化氢的电子式: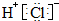 | ||
| C. | Cl2的结构式:Cl=Cl | D. | 硫离子的结构示意图: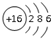 |
11.下列有关化学用语表达正确的是( )
| A. | Ar原子的结构示意图: | |
| B. | 丙烷分子的比例模型: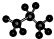 | |
| C. | NaClO的电子式: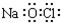 | |
| D. | HCO3-电离方程式:HCO3-+H2O?CO32-+H3O+ |
18.根据图示转化关系,下列说法不正确是( )
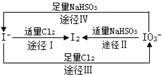

| A. | 由图可知离子还原性的强弱顺序为HSO3->I->Cl- | |
| B. | 足量Cl2能使湿润的淀粉-KI试纸先变蓝后变白 | |
| C. | 途径Ⅱ、Ⅳ反应后溶液的pH均减小 | |
| D. | 途径Ⅲ中若氧化1 mol I-,需消耗67.2L氯气 |
8.下列离子方程式不正确的是( )
| A. | 含有等物质的量的氢氧化钡、明矾两种溶液混合:3Ba2++6OH-+2Al3++3SO42-═3BaSO4+2Al(OH)3↓ | |
| B. | 纯碱溶液与胆矾溶液混合生成正盐、酸式盐、碱式盐:3CO32-+2Cu2++2H2O═2HCO3-+Cu2(OH)2CO3↓ | |
| C. | H218O中投入Na2O2固体:2H218O+2O22-═4OH-+18O2↑ | |
| D. | 0.1mol•L-1CuCl2溶液中加入0.1mol•L-1NaHS溶液:Cu2++HS-═CuS↓+H+ |
15.鸡舍中常不断地产生氨气.在大规模养鸡场中,氨气常引发鸡群出现呼吸道疾病,甚至会造成鸡的大批死亡.下列物质不适合于吸收氨气的是( )
| A. | 硫酸溶液 | B. | 醋酸溶液 | C. | Na0H固体 | D. | 硝酸溶液 |
10.在无色透明的溶液中能大量共存的一组离子是( )
| A. | H+、Fe3+、SO42-、Br- | B. | Ba2+、Na+、OH-、MnO4- | ||
| C. | H+、Na+、NO3-、Cl- | D. | Al3+、K+、HCO3-、OH- |
