题目内容
在化工生产中,常用MnS(s)作沉淀剂处理含Cu2+的废水。其反应原理为:Cu2+(aq)+MnS(s) CuS(s)+Mn2+(aq)。下列有关该反应的推理不正确的是
CuS(s)+Mn2+(aq)。下列有关该反应的推理不正确的是
A.该反应达到平衡时:c(Cu2+)=c(Mn2+)
B.CuS的溶解度比MnS的溶解度小
C.往平衡体系中加入少量Cu(NO3)2(s)后,c( Mn2 +)变大
D.该反应平衡常数表达式:
A
【解析】
试题分析:A、平衡时c(Cu2+)、c(Mn2+)均不在发生变化,但二者不一定相等,A错误;B、MnS能转化为CuS,根据沉淀容易向更难溶的方向转化可知,CuS的溶解度比MnS的溶解度小,B正确;C、往平衡体系中加入少量Cu(NO3)2(s)后,铜离子浓度增大,平衡向逆反应方向进行,则c( Mn2 +)变大,C正确;D、根据方程式可知该反应平衡常数表达式K= ,D正确,答案选A。
,D正确,答案选A。
考点:考查溶解平衡的应用

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案关于如图所示①、②两个装置的评价正确的是
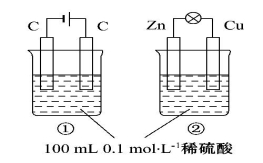
选择 | 叙 述 | 评价 |
A | 装置名称:①电解池,②原电池 | 错误 |
B | 硫酸浓度变化:①增大,②减小 | 错误 |
C | 电极反应式 ②正极:Zn-2e-====Zn2+ :①阳极:4OH--4e-====2H2O+O2↑ | 正确 |
D | 离子移动方向:①H+向阴极移动 ②H+向正极移动 | 正确 |
(16分)已知:乙二酸(HOOC-COOH,可简写为H2C2O4),俗称草酸,157℃时开始分解。
(1)探究草酸的酸性
25℃ H2C2O4 K1 = 5.4×10-2,K2 = 5.4×10-5 ;H2CO3 K1=4.5×10-7 K2= 4.7×10-11
下列化学方程式可能正确的是 。
A.H2C2O4 + CO32- = HCO3- + HC2O4-
B.HC2O4- + CO32- = HCO3- + C2O42-
C.2C2O42- + CO2 + H2O = 2HC2O4- + CO32-
D.H2C2O4 + CO32- = C2O42- + H2O +CO2↑
(2)探究草酸分解产物

实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用是 ,证明有CO气体生成的现象是 。
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加入4mL 0.01mol/L KMnO4酸性溶液2mL 0.1mol/L H2C2O4溶液, 再向乙试管中加入一粒黄豆大的MnSO4固体,摇匀。填写下表:
反应现象 | |
实验结论 | |
试管中发生反应的离子方程式 |
(4)用酸性KMnO4溶液滴定Na2C2O4,求算Na2C2O4的纯度
实验步骤:准确称取2.0g Na2C2O4固体,配成100mL溶液;取出20.00mL于锥形瓶中,再向瓶中加入足量稀H2SO4;用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL。
① 高锰酸钾溶液应装在_______滴定管中。(填“酸式”或“碱式”)
② Na2C2O4的纯度是______________。
 时,反应的离子方程式为_________________________
时,反应的离子方程式为_________________________
 Cl-
Cl-



