题目内容
7.下列各组中的离子,能在溶液中大量共存的是( )| A. | H+、Na+、OH-、SO42- | B. | Na+、Ca2+、CO32-、NO3- | ||
| C. | K+、H+、SO42-、Al3+ | D. | Na+、H+、Cl-、HCO3- |
分析 A.氢离子与氢氧根离子反应;
B.钙离子与碳酸根离子反应生成碳酸钙沉淀;
C.四种离子之间不反应,能够共存;
D.氢离子与碳酸氢根离子反应.
解答 解:A.H+、OH-之间发生反应,在溶液中不能大量共存,故A错误;
B.Ca2+、CO32-之间反应生成碳酸钙沉淀,在溶液中不能大量共存,故B错误;
C.K+、H+、SO42-、Al3+之间不反应,在溶液中能够大量共存,故C正确;
D.H+、HCO3-之间发生反应,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
17.下列各组物质的溶液,不用其他试剂通过互滴即可鉴别的是( )
①NaOH、MgCl2、AlCl3、K2SO4 ②CuSO4、Na2CO3、Ba(OH)2、H2SO4
③HNO3、NaAlO2、NaHSO4、NaCl ④NaOH、(NH4)2CO3、BaCl2、MgSO4.
①NaOH、MgCl2、AlCl3、K2SO4 ②CuSO4、Na2CO3、Ba(OH)2、H2SO4
③HNO3、NaAlO2、NaHSO4、NaCl ④NaOH、(NH4)2CO3、BaCl2、MgSO4.
| A. | ①② | B. | ①③ | C. | ①②④ | D. | ①③④ |
18.化学与人类生成、生活密切相关,下列有关说法错误的为( )
| A. | 以淀粉为原料可以制取乙酸乙酯 | |
| B. | 福尔马林可用于浸制标本,是因为其能使蛋白质变性 | |
| C. | 医用酒精通常是指体积分数为75%的乙醇溶液 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
15.在蒸发皿中加热蒸干再加热(低于400℃)下列物质的溶液可以得到该物质固体的是( )
| A. | 氯化铝 | B. | 碳酸氢钠 | C. | 高锰酸钾 | D. | 硫酸钠 |
2.下列有关化学与生活、工业的叙述中,不正确的是( )
| A. | 工业生产玻璃、水泥、漂白粉及用铁矿石冶炼铁,均需要用石灰石为原料 | |
| B. | CO会与血红蛋白结合,使人中毒;可将中毒病人放入高压氧仓中解毒,其解毒原理符合平衡移动原理 | |
| C. | 2011年5月份起,面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于碱性氧化物,过氧化苯甲酰属于有机物 | |
| D. | 固体煤经处理变为气体燃料后,可以减少SO2和烟尘的排放,且燃烧效率提高,有利于“节能减排” |
19.下列各组离子在溶液中能大量共存的是( )
| A. | 酸性溶液Na+、K+、MnO4-、Fe2+ | B. | 酸性溶液Fe3+、NH4+、SCN-、NH3+ | ||
| C. | 碱性溶液Na+、K+、AlO2-、SO42- | D. | 碱性溶液Ba2+、Na+、HCO3-、Cl- |
16.“绿色汽车”是指使用液化石油气等无污染或污染小的能源作燃料的汽车可有效减少有毒的铅、苯的同系物以及稠环芳烃的排放.燃烧等质量的液化石油气(主要成分是含C3~C4的烃)与汽油比较,最突出的优点是( )
| A. | 前者生成的水少 | B. | 前者对环境的污染小 | ||
| C. | 前者燃烧产生的热量多 | D. | 前者消耗氧气量少 |
17.下列图象能正确表示相关反应中产物物质的量的变化的是(横,纵坐标单位:mol)( )
| A. | 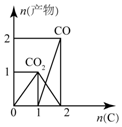 图:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物 | |
| B. | 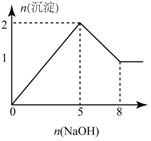 图:向含有1molMgCl2和1molAlCl3混合溶液中滴加NaOH,产生沉淀物质的量 | |
| C. | 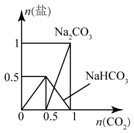 图:n(NaOH)=1mol,CO2逐步通入到NaOH溶液中反应生成的盐 | |
| D. | 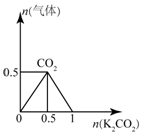 图:n(HCl)=1mol,K2CO3逐步加入到HCl溶液中,在敲口容器中生成的气体 |