题目内容
下列叙述或数据正确的是( )
| A、用广泛pH试纸测得某溶液的pH为2.3 |
| B、酸碱中和滴定实验中,锥形瓶必须用待测液润洗 |
| C、用已知浓度的盐酸滴定未知浓度的NaOH溶液时,若读取标准液读数时,滴前仰视,滴定到终点后俯视,会导致测定结果偏低 |
| D、用25mL滴定管进行中和滴定时,用去标准液的体积为21.7mL |
考点:试纸的使用,中和滴定
专题:实验评价题
分析:A.广泛pH试纸测得某溶液的pH只能为整数;
B.根据c(待测)=
分析误差;
C.利用c(碱)=
来进行误差分析;
D.滴定管0刻度在上方,自下而上刻度逐渐减小,每个小刻度为0.1mL,读数读到0.01mL;
B.根据c(待测)=
| C(标准)×V(标准) |
| V(待测) |
C.利用c(碱)=
| c(酸)V(酸) |
| V(碱) |
D.滴定管0刻度在上方,自下而上刻度逐渐减小,每个小刻度为0.1mL,读数读到0.01mL;
解答:
解:A.用广泛pH试纸测得某溶液的pH只能为整数,无法测定出读数为2.3的溶液的pH,故A错误;
B.锥形瓶用待测液润洗,待测液的物质的量增多,造成V(标准)偏大,根据c(待测)=
,可知c(标准)偏大,则测得待测液的浓度偏小,故B错误;
C.读取盐酸体积时,开始仰视读数,读数偏小,滴定结束时俯视读数,读数偏大,则差偏小,即消耗酸的体积偏小,所以c(碱)偏低,故C正确;
D.滴定管每个小刻度为0.1mL,读数读到0.01mL,用25mL滴定管进行中和滴定时,用去标准液的体积为21.7mL错误,故D错误;
故选C.
B.锥形瓶用待测液润洗,待测液的物质的量增多,造成V(标准)偏大,根据c(待测)=
| C(标准)×V(标准) |
| V(待测) |
C.读取盐酸体积时,开始仰视读数,读数偏小,滴定结束时俯视读数,读数偏大,则差偏小,即消耗酸的体积偏小,所以c(碱)偏低,故C正确;
D.滴定管每个小刻度为0.1mL,读数读到0.01mL,用25mL滴定管进行中和滴定时,用去标准液的体积为21.7mL错误,故D错误;
故选C.
点评:本题考查中和滴定,明确滴定实验中的仪器、数据处理及中和滴定的误差分析是解答本题的关键,注意掌握常见计量仪器的构造及其正确使用方法,如滴定管0刻度在上方,下方的大刻度以下还有一段没有刻度的部分,读数读到0.01mL,题目难度不大.

练习册系列答案
相关题目
我国稀土资源丰富.稀土元素
Sm原子核内中子数为( )
144 62 |
| A、62 | B、144 |
| C、206 | D、82 |
硅及其化合物在材料领域中应用广泛,下列叙述错误的是( )
| A、石英(SiO2)是制造玻璃的重要原料之一 |
| B、石英砂可以用于制取高纯度的硅,硅是将太阳能转化为电能的常用材料 |
| C、Na2SiO3是制备硅胶和木材防火剂的原料 |
| D、晶体硅是制造光导纤维的材料 |
下列离子方程式书写正确的是( )
| A、NaHCO3溶液中加入NaOH 溶液:HCO3-+OH-═CO2↑+H2O |
| B、在NaOH溶液中滴入少量AlCl3溶液:Al3++3OH-═Al(OH)3↓ |
| C、甲酸溶液中滴入NaOH溶液:HCOOH+OH-═HCOO-+H2O |
| D、CO2通入CaCl2溶液:CO2+H2O+Ca2+═CaCO3↓+2H+ |
五种短周期元素的原子半径及主要化合价如下,下列叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.104 | 0.111 | 0.066 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、R的氧化物及其对应的水化物均具有两性 |
| B、L、M的单质均用电解其熔融盐的方法冶炼 |
| C、T的氢化物还原性及稳定性均比Q的氢化物强 |
| D、五种元素的常见简单离子中半径最大的是Q2- |
下面是一种三肽,它可以看作是3个氨基酸缩合而得到的产物
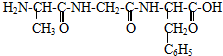
现有一个多肽分子,分子式为CXHYN12OD(X,Y,D为自然数)将它完全水解后只得到下列三种氨基酸
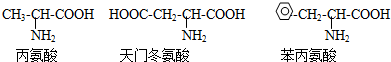
现将一个该多肽分子水解后,得到天门冬氨酸的分子个数为( )
现有一个多肽分子,分子式为CXHYN12OD(X,Y,D为自然数)将它完全水解后只得到下列三种氨基酸
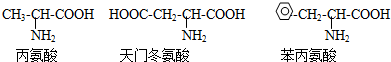
现将一个该多肽分子水解后,得到天门冬氨酸的分子个数为( )
| A、D-12 | ||
| B、D-13 | ||
C、
| ||
D、
|