题目内容
5.重结晶过程中,如果溶剂对杂质的溶解很少,对有机物的溶解性较强,那么在加入溶剂后进行过滤时( )| A. | 有机物在滤液中 | B. | 杂质在滤液中 | C. | 有机物滤纸上 | D. | 杂质在溶剂中 |
分析 溶剂对杂质的溶解很少,对有机物的溶解性较强,在过滤时会导致杂质不能透过滤纸,有机物能透过滤纸,据此分析解答.
解答 解:溶剂对杂质的溶解很少,对有机物的溶解性较强,在过滤时会导致杂质不能透过滤纸,有机物能透过滤纸,则有机物在滤液中、杂质在滤纸上,故选A.
点评 本题以过滤为载体考查物质分离和提纯,为高频考点,侧重考查学生获取信息利用信息解答问题能力,正确获取题干信息是解本题关键,会根据物质性质的差异性选取合适的分离提纯方法,题目难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
15.有0.1mol•L-1的三种溶液:①CH3COOH ②NaOH ③CH3COONa,下列说法正确的是( )
| A. | 溶液①、②等体积混合,混合液中c(CH3COO-)等于溶液③中的c(CH3COO-) | |
| B. | 溶液①、②等体积混合,混合液中c(CH3COO-)+c(CH3COOH)=0.1mol/L | |
| C. | 溶液①、③等体积混合,混合液中c(CH3COO-)+c(CH3COOH)=c(Na+) | |
| D. | 溶液①、③等体积混合,混合液中c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
16.在体积均为1.0L的两个恒容密闭容器中加入足量相同的碳粉,再分别充入0.1molCO2和0.2molCO2,在不同温度下发生反应CO2(g)+c(s)?2CO(g)达到平衡,平衡时c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )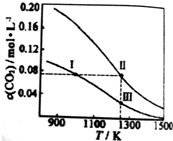

| A. | 反应CO2(g)+c(s)?2CO(g)△H<0 | |
| B. | 反应速率:V逆(状态Ⅰ)>V逆(状态Ⅲ) | |
| C. | 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ) | |
| D. | 体系的压强:2P总(状态Ⅰ)>P总(状态Ⅱ)>P总(状态Ⅰ) |
13.NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 室温下向1 L pH=1的醋酸溶液中加水,所得溶液的H+数目大于0.1NA | |
| B. | 60g乙酸与足量乙醇发生酯化反应,充分反应后断裂的C-O键数目为NA | |
| C. | 某无水乙醇与足量金属钠反应生成5.6 L H2,该乙醇分子中共价键总数为4 NA | |
| D. | 已知C2H4(g)+H2(g)═C2H6(g)△H=-137.0 kI/mol,乙烯与H2加成时放出68.5 kJ热量,则反应过程中被破坏的碳原子之间共用电子对数目为NA |
8.在恒温条件下,向容器中充入N2O4发生如下反应:N2O4(g)?2NO2 (g) 达到平衡时.(1)保持压强不变,再向容器内通入一定量的N2O4,重新达到平衡Ⅰ;(2)保持容器体积不变,再向容器内通入一定量的N2O4重新达到平衡Ⅱ.平衡Ⅰ、平衡Ⅱ与原平衡相比,N2O4的转化率( )
| A. | 不变、减小 | B. | 增大、减小 | C. | 减小、增大 | D. | 不变、增大 |
5.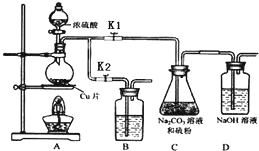 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.
已知:
①Na2S2O3在酸性溶液中不能稳定存在;
②硫代硫酸钠与碘反应的离子方程式为:2S2O32-+I2→S4O62-+2I-
(Ⅰ)制备Na2S2O3•5H2O
①打开K1,关闭K2,向放有铜片的圆底烧瓶中加入足量浓硫酸,加热.圆底烧瓶中发生反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
②C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.
C中碳酸钠的作用是提供碱性环境,作反应物.D中可能发生的离子反应方程式为:SO2+2OH-=SO32-+H2O、CO2+2OH-=CO32-+H2O.“停止C中的反应”的操作
是打开K2,关闭K1.
③过滤C中的混合液.将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.
④装置B中盛放的试剂是(填化学式)NaOH溶液,其作用是在C中的反应停止后,吸收A中产生的多余SO2,防止空气污染.
(Ⅱ)用I2的标准溶液测定产品的纯度取5.5g产品,配制成100mL溶液.取10.00mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如下表所示.
滴定时,达到滴定终点的现象是加入最后一滴I2标准溶液后,溶液变蓝,且半分钟内颜色不改变.Na2S2O3•5H2O在产品中的质量分数是90.2%(用百分数表示,且保留1位小数).
 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:
①Na2S2O3在酸性溶液中不能稳定存在;
②硫代硫酸钠与碘反应的离子方程式为:2S2O32-+I2→S4O62-+2I-
(Ⅰ)制备Na2S2O3•5H2O
①打开K1,关闭K2,向放有铜片的圆底烧瓶中加入足量浓硫酸,加热.圆底烧瓶中发生反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
②C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.
C中碳酸钠的作用是提供碱性环境,作反应物.D中可能发生的离子反应方程式为:SO2+2OH-=SO32-+H2O、CO2+2OH-=CO32-+H2O.“停止C中的反应”的操作
是打开K2,关闭K1.
③过滤C中的混合液.将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.
④装置B中盛放的试剂是(填化学式)NaOH溶液,其作用是在C中的反应停止后,吸收A中产生的多余SO2,防止空气污染.
(Ⅱ)用I2的标准溶液测定产品的纯度取5.5g产品,配制成100mL溶液.取10.00mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如下表所示.
| 编号 | 1 | 2 | 3 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.95 | 17.10 | 20.05 |
6.同温同压下,等质量的SO2和CO2相比较,下列叙述正确的是( )
| A. | 体积比1:1 | B. | 体积比11:16 | C. | 分子个数比1:1 | D. | 密度比11:16 |
 ②
②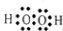 ③
③ ④
④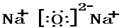 ⑤
⑤ ⑥
⑥ ⑦
⑦