题目内容
7.有关下列装置说法正确的是( )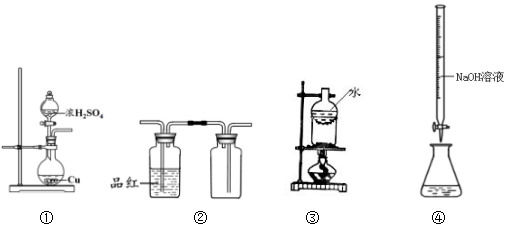
| A. | 用装置①制备SO2 | B. | 用装置②检验和收集SO2 | ||
| C. | 用装置③分离NaCl和I2 | D. | 用装置④测定溶液中c(H+) |
分析 A.Cu与浓硫酸反应需要加热;
B.二氧化硫可使品红褪色,但密度比空气密度大;
C.碘易升华,而NaCl不能;
D.NaOH与二氧化硅反应,图中为酸式滴定管.
解答 解:A.Cu与浓硫酸反应需要加热,则图中装置不能制备二氧化硫,故A错误;
B.二氧化硫可使品红褪色,但密度比空气密度大,图中收集方法不合理,故B错误;
C.碘易升华,而NaCl不能,则图中装置可分离,故C正确;
D.NaOH与二氧化硅反应,图中为酸式滴定管,应选碱式滴定管,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、物质的制备、混合物分离提纯、中和滴定为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
17.下列说法正确的是( )
| A. | 绿色植物的光合作用是把热能转化为化学能的过程 | |
| B. | 生物质能是与化学反应无关的一种能源 | |
| C. | 物质燃烧一定是放热反应 | |
| D. | 化学能只能以热能的形式释放 |
15.下列有机物命名正确的是( )
| A. | 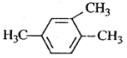 1,3,4-三甲苯 1,3,4-三甲苯 | B. | 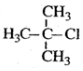 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | C. | 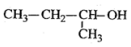 2-甲基-1-丙醇 2-甲基-1-丙醇 | D. | 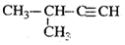 2-甲基-3-丁炔 2-甲基-3-丁炔 |
2.下列实验操作,对实验结果不产生影响的是( )
| A. | 在淀粉溶液中加入稀硫酸加热一段时间后,再滴加银氨溶液检验淀粉的水解产物 | |
| B. | 测定中和反应的反应热时,将碱溶液缓慢倒入酸溶液中 | |
| C. | 用蒸馏水湿润pH试纸后测定硫酸钠溶液的pH | |
| D. | 用酸碱中和滴定法测定未知浓度的碱液时,在锥形瓶中加入2-3mL酚酞试液作指示剂 |
19.下列关于有机化合物的说法正确的是( )
| A. | 聚氯乙烯分子中含碳碳双键 | B. | 乙醇、苯和溴苯用水即可鉴别 | ||
| C. | 汽油、柴油、植物油都是碳氢化合物 | D. | 油脂的皂化反应属于加成反应 |
16.已知20℃时,将5mL 0.1mol•L-1的Na2S3O3溶液和等体积、等浓度的稀H2SO4混合,9min后溶液中明显出现浑浊;50℃时,同样的反应要明显看到浑浊,仅需20s的时间.则温度每升高10℃,反应速率增大到原来的( )
| A. | 5倍 | B. | 4倍 | C. | 3 倍 | D. | 2倍 |
7.已知E1=134kJ/mol、E2=368kJ/mol,请参考题中图表,按要求填空: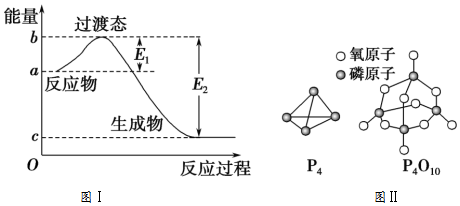
(1)图Ⅰ是1mol NO2(g)和1mol CO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,NO2和CO反应的热化学方程式为:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234kJ•mol-1.
(2)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用.目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应.
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)?(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)?NH4HCO3(aq)△H2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)?2NH4HCO3(aq)△H3
则△H3与△H1、△H2之间的关系是:△H3=2△H2-△H1.
(3)下表所示是部分化学键的键能参数:
已知白磷的燃烧热为d kJ/mol,白磷及其完全燃烧生成的产物的结构如图Ⅱ所示,表中x=$\frac{1}{4}$(6a+5c+d-12b) kJ/mol(用含a、b、c、d的代数式表示).

(1)图Ⅰ是1mol NO2(g)和1mol CO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,NO2和CO反应的热化学方程式为:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234kJ•mol-1.
(2)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用.目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应.
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)?(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)?NH4HCO3(aq)△H2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)?2NH4HCO3(aq)△H3
则△H3与△H1、△H2之间的关系是:△H3=2△H2-△H1.
(3)下表所示是部分化学键的键能参数:
| 化学键 | P-P | P-O | O═O | P═O |
| 键能/(kJ/mol) | a | b | c | x |