题目内容
15.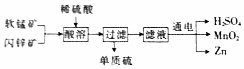 工业上可用软锰矿(主要成分MnO2)和闪锌矿(主要成分为ZnS)制备干电池中所需的MnO2和Zn,其工艺流程如图所示,下列说法中错误的是( )
工业上可用软锰矿(主要成分MnO2)和闪锌矿(主要成分为ZnS)制备干电池中所需的MnO2和Zn,其工艺流程如图所示,下列说法中错误的是( )| A. | 上述流程中锰元素的价态没有变化 | |
| B. | 上述流程中的硫酸可循环利用 | |
| C. | 通电过程中,生成Zn单质时发生还原反应 | |
| D. | 通电过程中,阳极的电极反应式为Mn2+-2e-+2H2O═MnO2+4H+ |
分析 软锰矿和闪锌矿加入硫酸,发生氧化还原反应可生成硫、硫酸锌和硫酸锰,过滤得到硫,滤液中含有硫酸锰、硫酸锌和硫酸,电解,得到锌、二氧化锰和硫酸,以此解答该题.
解答 解:A.二氧化锰在酸溶后被还原为锰离子,通电电解在阳极生成二氧化锰,元素化合价发生变化,故A错误;
B.酸溶后在最后电解滤液时又生成,可以循环利用,故B正确;
C.溶液中含有硫酸锌,生成锌单质,元素化合价降低,被还原,故C正确;
D.锰离子被氧化生成二氧化锰,为阳极反应,电极方程式为Mn2+-2e-+2H2O═MnO2+4H+,故D正确.
故选A.
点评 本题考查工业流程的分析判断,为高频考点,侧重于学生的分析能力和实验能力的考查,题目涉及电解原理的应用,注意把握物质的性质,题目难度中等.

练习册系列答案
相关题目
6.室温下,浓度均为0.5mol•L-1相同体积的下列四种溶液,其中所含阳离子数由多到少的顺序是( )
①KCl ②FeCl3③HF ④Na2CO3.
①KCl ②FeCl3③HF ④Na2CO3.
| A. | ④>①=②>③ | B. | ①>④>②>③ | C. | ④>①>③>② | D. | ④>②>①>③ |
3.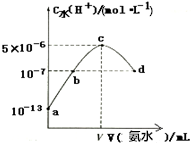 常温下,向20mL某浓度的硫酸中滴入0.1mol•L-1氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图所示.下列分析正确是( )
常温下,向20mL某浓度的硫酸中滴入0.1mol•L-1氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图所示.下列分析正确是( )
 常温下,向20mL某浓度的硫酸中滴入0.1mol•L-1氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图所示.下列分析正确是( )
常温下,向20mL某浓度的硫酸中滴入0.1mol•L-1氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图所示.下列分析正确是( )| A. | 该硫酸的浓度为1mol•L-1 | |
| B. | b点所示溶液中:c(NH4+)=2c(SO42-) | |
| C. | V=40 | |
| D. | c点所示溶液中:c(H+)-c(OH-)═c(NH3•H2O) |
10.向氯化亚铁溶液中加入过量的氨水,有沉淀生成.过滤.加热沉淀物至质量不再发声变化,得到红棕色的残渣.上述沉淀和残渣分别为( )
| A. | Fe(OH)2、Fe(OH)3;Fe3O4 | B. | Fe(OH)2;FeO | ||
| C. | Fe(OH)2、Fe(OH)3;Fe2O3 | D. | Fe2O3;Fe(OH)3 |
20.下列烃的名称中正确的是( )
| A. | 2-甲基-2-乙基戊烷 | B. | 3-甲基--己烯 | ||
| C. | 2-甲基-4-庚炔 | D. | 1,2,4-三甲苯 |
7.某溶液中Cl-、Br-、I-的物质的量之比为2:3:4.要使溶液中的Cl-、Br-、I-离子数之比变为4:3:2,则通入Cl2的分子数是原溶液中I-离子个数的( )
| A. | $\frac{1}{2}$ | B. | $\frac{1}{3}$ | C. | $\frac{1}{4}$ | D. | $\frac{1}{5}$ |
4.在恒温恒容密闭容器中充入0.5molN2和1.5molH2发生反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol充分反应后,下列说法正确的是( )
| A. | 在和上面初始体积相同的恒温恒压密闭容器中,也充入0.5molN2和1.5molH2发生反应则达到平衡时,放出的热量大于46.2kJ | |
| B. | 在平衡时再充入1molNH3则平衡向左移动,则平衡时N2的百分含量减小 | |
| C. | 若向容器中充入一定量He气,则平衡向右移动 | |
| D. | 在平衡后再充入1molH2,则N2的转化率增大,且平衡常数增大 |
5.化学与生活、环境、材料和科技等密切相关,表中对应关系错误的是( )
| 材料 | 主要化学成分 | |
| A | 水垢 | 碳酸钙 |
| B | 刚玉、钻石 | 三氧化二铅 |
| C | 古代陶瓷、普通玻璃 | 硅酸盐 |
| D | 水晶、硅藻土 | 二氧化硅 |
| A. | A | B. | B | C. | C | D. | D |
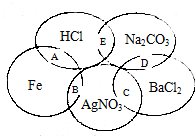 如图为一五元环图案,小明在图案上依次写了五种物质,图中相交的两种物质均可发生化学反应,A、B、C、D、E表示其相应的化学反应.请回答下列问题:
如图为一五元环图案,小明在图案上依次写了五种物质,图中相交的两种物质均可发生化学反应,A、B、C、D、E表示其相应的化学反应.请回答下列问题: