题目内容
16.在一个容积固定的反应容器中有一可左右滑动的密封隔板,将反应容器分甲、乙两室,甲室充入的是氢气与氯气,共2mol,乙室充入的是一氧化碳与氧气也共2mol,在一定条件下充分反应恢复到起始状态,反应前后变化如图所示:则起始时乙中一氧化碳与氧气的体积比可能为( )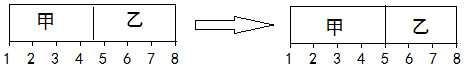
| A. | 1:2 | B. | 4:3 | C. | 2:1 | D. | 3:1 |
分析 H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,这是一个气体体积不变的反应,故混合气的总物质的量仍为2mol,2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2,反应后活塞停留在容器的$\frac{4}{7}$处,根据气体的物质的量之比等于体积之比,进行计算一氧化碳与氧气的体积比.
解答 解:H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,这是一个气体体积不变的反应,故混合气的总物质的量仍为2mol,2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2,反应后活塞停留在容器的$\frac{4}{7}$处.根据气体的物质的量之比等于体积之比,设一氧化碳与氧气反应后气体总物质的量为nmol,则$\frac{2mol}{n}=\frac{4}{3}$,则n=1.5mol,
若氧气充足2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2~△n=1mol(注意计算时以不足的作为计算对象)
2 1
1 2-1.5,则n(CO)=1mol,n(O2)=2mol-1mol=1mol,故一氧化碳与氧气的体积比为1:1;
若氧气不足2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2~△n=1mol(注意计算时以不足的作为计算对象)
1 1
0.5 2-1.5,则n(O2)=0.5mol,n(CO)=2mol-0.5mol=1.5mol,故一氧化碳与氧气的体积比为3:1,
故选D.
点评 本题考查了阿伏伽德罗定律及其推论,明确气体体积与物质的量的关系是解本题关键,注意平衡状态时两边容器内压强相等,题目难度中等.

| A. | 简单离子半径:W>Y>Z | B. | 气态氢化物的沸点:Y>W | ||
| C. | Y与W可以形成多种二元化合物 | D. | p、q与r的化学键类型完全相同 |
| A. | 在坩埚中放入NaCl溶液,加热、蒸发得到NaCl晶体 | |
| B. | 用10 mL的量筒量取4.8 mL的盐酸 | |
| C. | 用托盘天平称取25.20 g NaCl | |
| D. | 用1000 mL容量瓶配制450 mL 0.1 mol•L-1的盐酸 |
| A. | 2N | B. | Fe | C. | 2H2O | D. | 2SO2 |
| A. | 0.125mol/L | B. | 0.175 mol/L | C. | 0.25 mol/L | D. | 0.50 mol/L |
(1)甲用如图装置进行实验(气密性已检验,加热和夹持装置已略去).实验进行一段时间后,C、D中都出现明显的白色沉淀,经检验均为BaSO4.
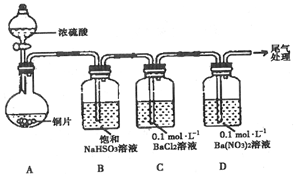
①A中反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
②为探究SO2在D中所发生的反应,甲进一步实验发现,出现白色沉淀的过程中,D溶液中NO3浓度几乎不变.甲据此得出结论:C、D中出现白色沉淀的主要原因是在酸性条件下,+4价硫被A(填序号)氧化成SO42-.
A.O2 B.Ba2+ C.NO3-
(2)乙用如下实验对含+4价硫元素的物质性质继续进行探究.(均在敞口容器中)
| 序号 | 实验操作 | 实验现象 |
| 1 | 取0.3g 纯净Na2SO3固体,向其中加入10mL 2mol•L-1 盐酸,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,4min后,溶液变浑浊 |
| 2 | 取0.3g 纯净Na2SO3固体,向其中加入10mL 2mol•L-1 HNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,2h后,溶液变浑浊 |
| 3 | 取0.3g 纯净Na2SO3固体,向其中加入10mL 浓HNO3,再滴入4滴BaCl2溶液 | 产生红棕色气体;滴入BaCl2溶液后,溶液立即产生大量白色沉淀 |
②由实验1、2、3对比,可以得到推论:含+4价硫元素物质可被O2和浓HNO3氧化.
③乙通过查阅资料发现:Na+对实验1和2中出现浑.浊的时间无影响,于是进一步探究Cl-和NO3-对其的影响:
| 序号 | 实验操作 | 实验现象 |
| 4 | 取0.3g纯净Na2SO3和1.17gNaCl固体混合物,向其中加入10mL 2mol•L-1 HNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,20min后,溶液变浑浊 |
ii.实验1和4对比,乙获得推论:NO3-的存在可以减慢溶液中+4价硫元素的氧化.
④通过以上实验,可以推测B装置最有可能的作用是吸收+6价硫的化合物.
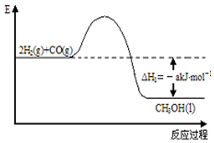 能源是人类生存和发展的重要支柱.研究并有效地开发新能源在能源紧缺的今天具有重要的理论意义.已知H2与CO反应生成CH3OH的过程如图所示:CO的燃烧热△H2=-b kJ•mol-1,CH3OH的燃烧热
能源是人类生存和发展的重要支柱.研究并有效地开发新能源在能源紧缺的今天具有重要的理论意义.已知H2与CO反应生成CH3OH的过程如图所示:CO的燃烧热△H2=-b kJ•mol-1,CH3OH的燃烧热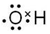 .
.