题目内容
12.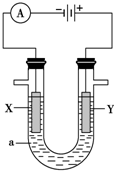 电解原理在化学工业中有广泛的应用.下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)若X、Y都是惰性电极,a是饱和MgCl2溶液,则:
①电解池中X极上的电极反应式为2H++2e-=H2↑,在X极附近观察到的现象是有气体和沉定生成.电解液中向X极方向移动的离子是Mg2+、H+.
②检验Y电极反应产物的方法是把湿润的淀粉碘化钾试纸放在Y电极附近,试纸变蓝色,说明生成了Cl2.
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是粗铜,电极反应式为Cu2++2e-═Cu.
②溶液中的c(Cu2+)与电解前相比变小(填“变大”、“变小”或“不变”).
(3)如利用该装置实现铁上镀银,电极Y上发生的反应为Ag-e-═Ag+,电解池盛放的电镀液可以是AgNO3溶液.
分析 (1)电解饱和氯化镁时,由电源可知,X为阴极,Y为阳极,阳极上是氯离子失电子,阴极上是氢离子得电子,以此解答该题;
(2)电解方法精炼粗铜,电解液a选用CuSO4溶液,粗铜做阳极,精铜做阴极;
(3)电镀时,镀层作阳极,镀件作阴极,含有镀层金属阳离子的盐溶液为电镀液.
解答 解:(1)①和电源的负极相连的电极X极是阴极,阳离子Mg2+、H+移向此电极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,该电极附近氢氧根离子浓度增加,产生氢氧化镁沉淀,故答案为:2H++2e-═H2↑;有气体和沉定生成;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,氯气可用淀粉碘化钾试纸检验,可使试纸变蓝色,故答案为:把湿润的淀粉碘化钾试纸放在Y电极附近,试纸变蓝色,说明生成了Cl2;
(2)电解方法精炼粗铜,电解液a选用CuSO4溶液,粗铜做阳极,精铜做阴极;
①Y电极为电解池的阳极,所以Y电极的材料是粗铜;X电极是阴极,电极材料是纯铜,该电极上发生反应:Cu2++2e-═Cu,
故答案为:纯铜;Cu2++2e-═Cu;
②该电解池的阳极材料是粗铜,参与放电的是金属锌、铁、铜等金属,在阴极上一直是铜离子得电子的还原反应,溶液中的c(Cu2+)与电解前相比减小,故答案为:变小;
(3)铁上镀银时,镀层金属银作阳极,发生反应:Ag-e-═Ag+,镀件金属铁作阴极,含有镀层金属阳离子银离子的盐溶液AgNO3溶液为电镀液,故答案为:Ag-e-═Ag+;AgNO3溶液.
点评 本题考查学生电解池的工作原理知识,明确图中电源的正负极确定电解池的阴阳极是解答的关键,并熟悉电极反应及离子的放电顺序来解答,题目难度中等.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
2.X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的化合物的焰色反应呈黄色,R原子的核外电子数是X原子与Z原子的核外电子数之和.下列叙述正确的是( )
| A. | 原子半径的大小顺序:r(X)>r(Y)>r(Z)>r(R) | |
| B. | 含有Y、Z、R三种元素的化合物最多只有2种 | |
| C. | 元素R和Y形成的化合物RY2是一种高效安全灭菌消毒剂 | |
| D. | Y与Z形成的两种化合物中的化学键和晶体类型均相同 |
20. 将CO2转化为 CH4,既可以减少温室气体的排放,又能得到清洁能源.已知:CO2(g)+2H2O(g)═CH4(g)+2O2(g)△H=+802kJ•mol-1如图为在恒温、光照和不同催化剂(Ⅰ、Ⅱ)作用下,体积为1L的密闭容器中n (CH4)随光照时间的变化曲线.下列说法正确的是( )
将CO2转化为 CH4,既可以减少温室气体的排放,又能得到清洁能源.已知:CO2(g)+2H2O(g)═CH4(g)+2O2(g)△H=+802kJ•mol-1如图为在恒温、光照和不同催化剂(Ⅰ、Ⅱ)作用下,体积为1L的密闭容器中n (CH4)随光照时间的变化曲线.下列说法正确的是( )
 将CO2转化为 CH4,既可以减少温室气体的排放,又能得到清洁能源.已知:CO2(g)+2H2O(g)═CH4(g)+2O2(g)△H=+802kJ•mol-1如图为在恒温、光照和不同催化剂(Ⅰ、Ⅱ)作用下,体积为1L的密闭容器中n (CH4)随光照时间的变化曲线.下列说法正确的是( )
将CO2转化为 CH4,既可以减少温室气体的排放,又能得到清洁能源.已知:CO2(g)+2H2O(g)═CH4(g)+2O2(g)△H=+802kJ•mol-1如图为在恒温、光照和不同催化剂(Ⅰ、Ⅱ)作用下,体积为1L的密闭容器中n (CH4)随光照时间的变化曲线.下列说法正确的是( )| A. | 0~16 h内,v(H2O)Ⅰ=1.5 mol/(L•h) | |
| B. | 0~25 h内,催化剂Ⅰ的催化效果比催化剂Ⅱ的效果好 | |
| C. | 在两种不同催化剂下,该反应的平衡常数不相等 | |
| D. | 反应开始后的15h内,第Ⅰ种催化剂的作用下,得到的CH4最多 |
7.在一定条件下,当64g SO2气体被氧化成SO3气体时,共放出热量98.3kJ,已知SO2在此条件下转化率为80%,据此,下列热化学方程式正确的是( )
| A. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98.3 kJ/mol | |
| B. | 2SO2(g)+O2(g)?SO3(l)△H=-196.6 kJ/mol | |
| C. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-122.9 kJ/mol | |
| D. | 2SO2(g)+O2(g)?SO3(g)△H=+196.6 kJ/mol |
4.下列除杂试剂、主要操作或方法均正确的是(括号内为杂质)( )
| 选项 | 原物质及杂质 | 除杂试剂 | 主要操作或方法 |
| A | 乙酸乙酯(乙酸) | Na2CO3 | 过滤 |
| B | Na2CO3(s )[NaHCO3(s )] | NaOH溶液 | 转化法 |
| C | FeCl2(CuCl2) | Zn | 过滤 |
| D | 苯(溴) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
1.工业制硝酸的主要反应是:4NH3(g)+5O2(g)?4NO(g)+6H2O (g)+1025kJ
(1)该反应的平衡常数表达式为$\frac{{c}^{4}(NO){c}^{6}({H}_{2}O)}{{c}^{4}(N{H}_{3}){c}^{5}({O}_{2})}$;升高温度K值减小 (填“增大”、“减小”或“不变”).
(2)若反应物起始的物质的量相同,下列关系图错误的是c (填字母序号).
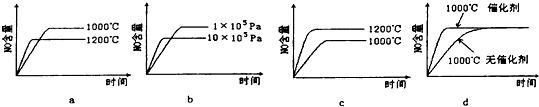
(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
①起始时物料比c (O2):c (NH3)>1.25,其原因是增大氨气的转化率.
②反应在第2min到第4min时O2的平均反应速率为0.1875;
③反应在第8min改变的反应条件可能是增大反应物的浓度.
(1)该反应的平衡常数表达式为$\frac{{c}^{4}(NO){c}^{6}({H}_{2}O)}{{c}^{4}(N{H}_{3}){c}^{5}({O}_{2})}$;升高温度K值减小 (填“增大”、“减小”或“不变”).
(2)若反应物起始的物质的量相同,下列关系图错误的是c (填字母序号).

(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.8 | 0.975 | 0.5 |
②反应在第2min到第4min时O2的平均反应速率为0.1875;
③反应在第8min改变的反应条件可能是增大反应物的浓度.
2.下列反应中,硝酸既表现氧化性又表现酸性的是( )
| A. | FeO和HNO3 | B. | Cu(OH)2和HNO3 | C. | CuO和HNO3 | D. | H2S和HNO3 |
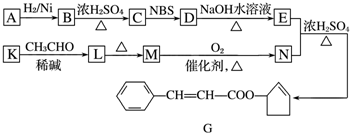
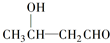
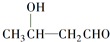 $\stackrel{△}{→}$CH3CH═CHCHO+H2O
$\stackrel{△}{→}$CH3CH═CHCHO+H2O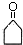 ,G中官能团的名称为碳碳双键和酯基.
,G中官能团的名称为碳碳双键和酯基. ,反应类型加成反应.
,反应类型加成反应.