题目内容
 Ⅰ.( 1)在一个体积为2L的密闭容器中充入6mol SO2和3mol O2,进行下列反应2SO2(g)+O2(g)?2SO3(g),保持温度不变,2min后达到平衡,测得混合气体中O2的体积分数为25%,用SO2浓度变化来表示的化学反应速率为
Ⅰ.( 1)在一个体积为2L的密闭容器中充入6mol SO2和3mol O2,进行下列反应2SO2(g)+O2(g)?2SO3(g),保持温度不变,2min后达到平衡,测得混合气体中O2的体积分数为25%,用SO2浓度变化来表示的化学反应速率为(2)如图A表示在密闭容器中反应:2SO2+O2?2SO3△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a-b过程中改变的条件可能是
(3)以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡后,容器内温度将
Ⅱ.图1是CO(g)+2H2(g)?CH3OH(g)反应在不同温度下CO的转化率随时间变化的曲线.
(1)反应的焓变△H
(2)T1和T2温度下的平衡常数大小关系是K1
(3)T1时,往体积为1L的密闭容器中,充入1mol CO和2mol H2,经测得CO和CH3OH(g)的浓度随时间变化如图2.则该反应的平衡常数为

(4)若容器容积不变,下列措施可增加CO转化率的是
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大.
考点:化学平衡的影响因素,物质的量或浓度随时间的变化曲线,转化率随温度、压强的变化曲线,化学反应速率和化学计量数的关系
专题:化学平衡专题
分析:Ⅰ、(1)依据化学平衡三段式列式计算,结合反应速率概念计算;
(2)根据正逆反应速率的变化结合温度、压强对反应速率和化学平衡的影响判断,a时逆反应速率大于正反应速率,且正逆反应速率都增大,b时正反应速率大于逆反应速率,注意逆反应速率突然减小的特点;
(3)若此时只将容器的体积扩大为原来的2倍,压强减小,平衡向气体体积增大的方向进行,平衡逆向进行,容器不与外界进行热交换,温度降低;
Ⅱ、(1)“先拐先平”温度高T2>T1,依据平衡移动原理结合一氧化碳转化率变化分析;
(2)图象分析“先拐先平”温度高T2>T1,依据平衡移动原理结合一氧化碳转化率变化分析平衡移动方向,得到平衡常数大小;
(3)依据图象分析平衡量,甲醇浓度为0.75mol/L,一氧化碳浓度为0.25mol/L,根据化学平衡三段式列式计算平衡浓度,结合平衡常数概念计算得到;
(4)若容器容积不变,下列措施可增加CO转化率,平衡正向进行,依据平衡移动原理分析判断.
(2)根据正逆反应速率的变化结合温度、压强对反应速率和化学平衡的影响判断,a时逆反应速率大于正反应速率,且正逆反应速率都增大,b时正反应速率大于逆反应速率,注意逆反应速率突然减小的特点;
(3)若此时只将容器的体积扩大为原来的2倍,压强减小,平衡向气体体积增大的方向进行,平衡逆向进行,容器不与外界进行热交换,温度降低;
Ⅱ、(1)“先拐先平”温度高T2>T1,依据平衡移动原理结合一氧化碳转化率变化分析;
(2)图象分析“先拐先平”温度高T2>T1,依据平衡移动原理结合一氧化碳转化率变化分析平衡移动方向,得到平衡常数大小;
(3)依据图象分析平衡量,甲醇浓度为0.75mol/L,一氧化碳浓度为0.25mol/L,根据化学平衡三段式列式计算平衡浓度,结合平衡常数概念计算得到;
(4)若容器容积不变,下列措施可增加CO转化率,平衡正向进行,依据平衡移动原理分析判断.
解答:
解:I、(1)在一个体积为2L的密闭容器中充入6mol SO2和3mol O2,进行下列反应2SO2(g)+O2(g)?2SO3(g),设消耗二氧化硫物质的量为x,
2SO2(g)+O2(g)?2SO3(g)
起始量(mol) 6 3 0
变化量(mol) x 0.5x x
平衡量(mol) 6-x 3-0.5x x
保持温度不变,2min后达到平衡,测得混合气体中O2的体积分数为25%,体积比等于物质的量之比,则
×100%=25%,解得x=2mol,用SO2浓度变化来表示的化学反应速率=
=0.5mol?L-1?min-1,
故答案为:0.5mol?L-1?min-1;
(2)a时逆反应速率大于正反应速率,说明平衡应向逆反应方向移动,且正逆反应速率都增大,该反应的正反应放热,应为升高温度的结果;b时正反应速率不变,逆反应速率减小,在此基础上逐渐减小,应为减小生成物的原因;增大压强,正逆反应速率都增大,平衡向气体体积减小的方向移动即正反应方向移动,因此正反应速率大于逆反应速率,图象应为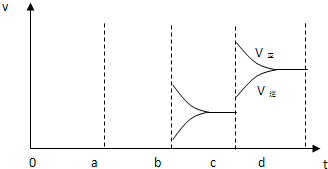 ,
,
故答案为:升高温度;减小SO3浓度; ;
;
(3)2SO2(g)+O2(g)?2SO3(g),反应是放热反应,若此时只将容器的体积扩大为原来的2倍,压强减小,平衡向气体体积增大的方向进行,即逆向移动,容器不与外界进行热交换,逆向吸热会导致温度降低,
故答案为:降低;
II、(1)由T2温度下反应速率斜率更大,反应速率更快,得出T2>T1,由图象可知一氧化碳转化率随温度升高减小,说明温度升高,平衡逆向进行,正反应为放热反应,△H<0,
故答案为:<;
(2)T2>T1,温度升高,平衡逆向进行,说明平衡常数K1>K2,
故答案为:>;
(3)T1时,往体积为1L的密闭容器中,充入1mol CO和2mol H2,经测得CO和CH3OH(g)的浓度随时间变化如图分析可知,甲醇浓度为0.75mol/L,一氧化碳浓度为0.25mol/L;
CO(g)+2H2(g)?CH3OH(g)
起始量(mol/L) 1 2 0
变化量(mol/L) 0.75 1.5 0.75
平衡量(mol/L) 0.25 0.5 0.75
平衡常数K=
=12,
故答案为:12;
(4)a.反应是放热反应,升高温度,平衡逆向进行,一氧化碳转化率减小,故a错误;
b.将CH3OH(g)从体系中分离,平衡正向进行,一氧化碳转化率增大,故b正确;
c.使用合适的催化剂,改变反应速率不改变平衡,一氧化碳转化率不变,故c错误;
d.充入He,使体系总压强增大,恒容容器中,参与反应的物质分压不变平衡不动,一氧化碳转化率不变,故d错误;
故答案为:b.
2SO2(g)+O2(g)?2SO3(g)
起始量(mol) 6 3 0
变化量(mol) x 0.5x x
平衡量(mol) 6-x 3-0.5x x
保持温度不变,2min后达到平衡,测得混合气体中O2的体积分数为25%,体积比等于物质的量之比,则
| 3-0.5x |
| 9-0.5x |
| ||
| 2min |
故答案为:0.5mol?L-1?min-1;
(2)a时逆反应速率大于正反应速率,说明平衡应向逆反应方向移动,且正逆反应速率都增大,该反应的正反应放热,应为升高温度的结果;b时正反应速率不变,逆反应速率减小,在此基础上逐渐减小,应为减小生成物的原因;增大压强,正逆反应速率都增大,平衡向气体体积减小的方向移动即正反应方向移动,因此正反应速率大于逆反应速率,图象应为
 ,
,故答案为:升高温度;减小SO3浓度;
 ;
;(3)2SO2(g)+O2(g)?2SO3(g),反应是放热反应,若此时只将容器的体积扩大为原来的2倍,压强减小,平衡向气体体积增大的方向进行,即逆向移动,容器不与外界进行热交换,逆向吸热会导致温度降低,
故答案为:降低;
II、(1)由T2温度下反应速率斜率更大,反应速率更快,得出T2>T1,由图象可知一氧化碳转化率随温度升高减小,说明温度升高,平衡逆向进行,正反应为放热反应,△H<0,
故答案为:<;
(2)T2>T1,温度升高,平衡逆向进行,说明平衡常数K1>K2,
故答案为:>;
(3)T1时,往体积为1L的密闭容器中,充入1mol CO和2mol H2,经测得CO和CH3OH(g)的浓度随时间变化如图分析可知,甲醇浓度为0.75mol/L,一氧化碳浓度为0.25mol/L;
CO(g)+2H2(g)?CH3OH(g)
起始量(mol/L) 1 2 0
变化量(mol/L) 0.75 1.5 0.75
平衡量(mol/L) 0.25 0.5 0.75
平衡常数K=
| 0.75 |
| 0.25×0.52 |
故答案为:12;
(4)a.反应是放热反应,升高温度,平衡逆向进行,一氧化碳转化率减小,故a错误;
b.将CH3OH(g)从体系中分离,平衡正向进行,一氧化碳转化率增大,故b正确;
c.使用合适的催化剂,改变反应速率不改变平衡,一氧化碳转化率不变,故c错误;
d.充入He,使体系总压强增大,恒容容器中,参与反应的物质分压不变平衡不动,一氧化碳转化率不变,故d错误;
故答案为:b.
点评:本题考查了化学平衡移动原理的分析判断,图象分析方法和平衡计算应用,注意平衡常数随温度变化,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
将一定温度下的饱和硝酸钾溶液变为不饱和溶液,可以采取的方法是( )
| A、升温或加水 |
| B、降温或加水 |
| C、升温或蒸发水 |
| D、降温或蒸发水 |
下列离子方程式正确的是( )
| A、氯气通入氢氧化钠溶液制消毒液:Cl2+2OH-=ClO-+Cl-+H2O |
| B、硫酸铜溶液与氢氧化钡溶液混合:SO42-+Ba2+=BaSO4↓ |
| C、碳酸氢钠与稀硫酸:CO32-+2H+=H2O+CO2↑ |
| D、二氧化碳气体通入过量氢氧化钠溶液:OH-+CO22-=HCO3- |
在用浓盐酸与二氧化锰共热制取氯气的反应中,消耗的HCl的物质的量与作还原剂的HCl的物质的量之比是( )
| A、1:1 | B、1:2 |
| C、2:1 | D、4:1 |

 已知硫酸工业生产过程中涉及的化学反应有:
已知硫酸工业生产过程中涉及的化学反应有: