题目内容
10.常温下为气态的烷烃A和炔烃B的混台气体,其密度是H2的27.5倍.已知A、B分子中含碳原子数相同.求:(1)A、B的分子式.
(2)A与B的体积之比.
(3)若在120℃和1.01×105Pa下将1L该混何合气体与9L O2混台后充入密闭容器中,点燃充分燃烧后又恢复到原来状况下,问此时气体总体积为多少升.
分析 (1)常温下为气态的烷烃A和炔烃B的混台气体,其密度是H2的27.5倍,则混合气体的平均分子量为27.5×2=55,设A的分子式为CnH2n+2,B的分子式为CnH2n-2,
由于A、B分子中含碳原子数相同.,所以A、B应该都含有4个碳原子,烷烃为丁烷,炔烃为丁炔;
(2)设丁烷的体积分数为x,丁炔的体积分数为y,根据混合气体的平均分子量计算;
(3)根据反应方程式CnH2n+2+($\frac{3n+1}{2}$)O2$\stackrel{点燃}{→}$nCO2+(n+1)H2O、CnH2n-2+($\frac{3n-1}{2}$)O2$\stackrel{点燃}{→}$nCO2+(n-1)H2O计算.
解答 解:(1)常温下为气态的烷烃A和炔烃B的混台气体,其密度是H2的27.5倍,则混合气体的平均分子量为27.5×2=55,设A的分子式为CnH2n+2,B的分子式为CnH2n-2,
由于A、B分子中含碳原子数相同,所以A、B应该都含有4个碳原子,烷烃为丁烷其分子式为C4H10,炔烃为丁炔其分子式为C4H6;
答:A、B的分子式分别为C4H10、C4H6;
(2)设丁烷的体积为x,丁炔的体积为y,已知混合气体的平均分子量为55;
$\frac{58x+54y}{x+y}$=55,则x:y=1:3;
答:A与B的体积之比为1:3;
(3)1L该混何合气体,丁烷为0.25L,丁炔为0.75L,
C4H10+6.5O2$\stackrel{点燃}{→}$4CO2+5H2O
0.25L 1.625L 1L 1.25L
C4H6+5.5O2$\stackrel{点燃}{→}$4CO2+3H2O
0.75L 4.125L 3L 2.25L
则反应后气体总体积为9L-1.625L-4.125L+1L+3L+1.25L+2.25L=10.75L;
答:反应后气体总体积为10.75L.
点评 本题考查了有机物分子式、结构简式的计算,题目难度中等,注意掌握确定有机物分子式的方法,明确质量守恒在计算中的应用,注意掌握解答方法,侧重于考查学生的分析能力和计算能力.

 阅读快车系列答案
阅读快车系列答案| A. | 体积为44.8L | B. | 含有4mol氧原子 | ||
| C. | 分子数为6.02×1023 | D. | 摩尔质量为128g |
| A. | 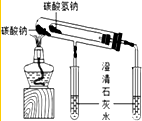 比较碳酸钠与碳酸氢钠的热稳定性 | B. |  称取NaOH | ||
| C. | 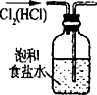 除去Cl2中HCl | D. | 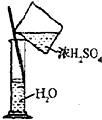 稀释浓H2SO4 |
①分液 ②蒸馏 ③过滤 ④盐析 ⑤渗析.
| A. | ①② | B. | ③④ | C. | ②③④ | D. | ②③⑤ |
| A. | 9g甲基(-CH3)所含有的电子数是10NA个 | |
| B. | 4.2gC3H6中含有的碳碳双键数一定为0.1NA | |
| C. | 常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 | |
| D. | 22.4L乙烷中含有的共价键数为7NA个 |
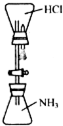 某同学受喷泉实验原理的启发,设计如图所示装置进行“喷烟”实验.下列对实验的有关说法错误的是( )
某同学受喷泉实验原理的启发,设计如图所示装置进行“喷烟”实验.下列对实验的有关说法错误的是( )| A. | 由于NH3的密度比HCl小,实验中二者的位置不能调换 | |
| B. | “白烟”是由于生成NH4Cl固体小颗粒的缘故 | |
| C. | 若用HBr代替HCl进行相同的操作,可得到相同的现象 | |
| D. | 实验时,打开活塞并挤出胶头滴管中的水即可看到白烟 |
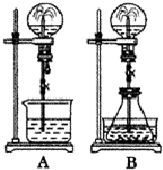 喷泉实验是一种常见的自然现象,其产生原因是存在压强差.试根据图,回答下列问题:
喷泉实验是一种常见的自然现象,其产生原因是存在压强差.试根据图,回答下列问题: