题目内容
7.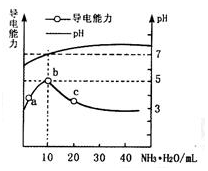 常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的NH3•H2O溶液,所得溶液pH及导电能力变化如图.下列分析不正确的是( )
常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的NH3•H2O溶液,所得溶液pH及导电能力变化如图.下列分析不正确的是( )| A. | a~b点导电能力增强,说明HR为弱酸 | B. | b点溶液pH=7,此时酸碱恰好中和 | ||
| C. | c点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+) | D. | b、c两点水的电离程度:b<c |
分析 A.根据图象可知,a~b点导电能力增强,说明HR为弱电解质,在溶液中部分电离,加入氨水后生成强电解质,离子浓度增大;
B.b点溶液pH=7,此时加入10mLHR,HR与一水合氨的浓度、体积相等,则二者恰好反应;
C.c点时溶液的pH>7,混合液显示碱性,则c(OH-)>c(H+),结合电荷守恒可知:c(NH4+)>c(R-);
D.酸或碱抑制水电离,且酸中c(H+)越大、碱中c(OH-)越大,其抑制水电离程度越大,含有弱离子的盐促进水电离.
解答 解:A.a~b点导电能力增强,说明反应后溶液中离子浓度增大,也证明HR在溶液中部分电离,为弱酸,故A正确;
B.体积图象可知b点溶液pH=7,此时HR与一水合氨的物质的量相等,二者恰好反应生成NH4R,故B正确;
C.根据图象可知,c点时溶液的pH>7,混合液呈碱性,则c(OH-)>c(H+),结合电荷守恒可知:c(NH4+)>c(R-),故C正确;
D.a点酸碱恰好中和,为弱酸弱碱盐,c点氨水过量,一水合氨抑制水的电离,则b、c两点水的电离程度:b>c,故D错误.
故选D.
点评 本题考查了酸碱混合的定性判断、离子浓度定性比较、溶液导电性及其影响等知识,题目难度中等,明确酸碱混合的定性判断及溶液酸碱性与溶液pH的计算方法为解答关键,试题侧重考查学生的分析、理解能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列关于${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl说法正确的是( )
| A. | 具有相同的质子数 | B. | 具有相同的中子数 | ||
| C. | 具有相同的质量数 | D. | 它们不互为同位素 |
15.下列有关实验的说法正确的是( )
| A. | 用pH试纸测双氧水的pH | |
| B. | 用酸式滴定管量取20.00 mL酸性KMnO4溶液 | |
| C. | 用托盘天平称取 5.85 g NaCl晶体 | |
| D. | 用带磨口玻璃塞的试剂瓶保存Na2CO3溶液 |
2.将氢气、甲烷、乙醇等物质在氧气中嫩烧时的化学能直接转化为电能的装置叫燃料电池.此种电池能量利用率可高达80%,产物污染也少.下列有关燃料电池说法错误的是( )
| A. | 上述燃料电池的负极反应材料是氢气、甲烷、乙醇等物质 | |
| B. | 氮氧燃料电池常用于肮天飞行器,原因之一是该电池的产物为水,经过处理之后可供宇肮员使用 | |
| C. | 乙醇燃料电池的常用KOH溶液,该电池的负极反应为C2H5OH-12e-+3H2O═CO2↑+12H+ | |
| D. | 甲烷碱性燃料电池工作时OH-定向移动到负极 |
12.利用下列装置不能完成对应实验的是( )
| A. |  实验室制取氨气 | B. | 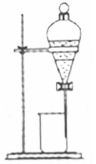 用CCl4萃取碘水中的碘 | ||
| C. | 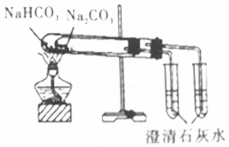 比较Na2CO3与NaHCO3的稳定性 | D. | 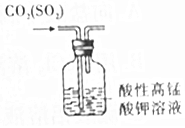 除去CO2中混有的少量SO2 |
19.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 干冰只能用于人工降雨 | |
| B. | Al(OH)3可以治疗胃酸过多,因此可大量使用 | |
| C. | 为了增强去污效果,在洗衣粉中添加三聚磷酸钠(Na5P3O10) | |
| D. | 侯氏制碱法不涉及基本反应类型中的置换反应 |
16.如表是短周期的一部分,Y原子的核电荷数是X的2倍,下列关于这四种元素的说法正确的是( )
| X | ||
| M | Y | Z |
| A. | 氢化物沸点最高的是H2X | B. | M4的摩尔质量为124 | ||
| C. | X、Y、Z的简单离子半径最大的是Z | D. | X、Y两种元素,化合价都可以显-1价 |