题目内容
1. 高温裂解法处理工业废硫酸的原理为:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ/mol,它由两步反应组成:
高温裂解法处理工业废硫酸的原理为:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ/mol,它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g)△H=+177kJ/mol
ii.SO3(g)分解.
(1)SO3(g)分解的热化学方程式为2SO3(g)=2SO2(g)+O2(g)△H=+196kJ/mol.
(2)工业上常用SO2制备Na2S2O3,向0.1mol/L的Na2S2O3溶液中滴加稀硫酸的离子方程式为S2O32-+2H+=S↓+SO2↑+H2O.
(3)反应ii的△S> 0 (填“>”、“<”、“=”).
(4)对反应ii,可用V2O5作催化剂. 已知:SO2+V2O5?SO3+V2O4K1、$\frac{1}{2}$O2+V2O4?V2O5K2,则在相同温度下,2SO3(g)?2SO2(g)+O2(g)的平衡常数 K=$\frac{1}{{{K}_{1}}^{2}•{{K}_{2}}^{2}}$(用K1、K2表示).
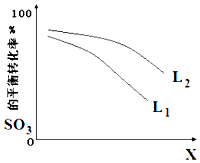
(5)L(L1、L2),X可分别代表压强或温度,如图表示L一定时,反应ii中SO3(g)的平衡转化率随X的变化关系.
①X代表的物理量是压强;
②比较L1、L2的大小L2>L1.
(6)维持体系总压p恒定,在T℃时,物质的量为9mol、体积为2L的SO3(g)发生反应:2SO3(g)?2SO2(g)+O2(g),已知SO3的平衡转化率25%,则在该温度下反应的平衡常数K=$\frac{1}{18}$mol/L(用最简分数表示).
分析 (1)已知:①2H2SO4(l)═2SO2(g)+O2(g)+2H2O(g)△H=+550kJ•mol-1
②H2SO4(l)═SO3(g)+H2O(g)△H=+177kJ•mol-1
根据盖斯定律①-2×②可得;
(2)根据化合价分析用Na2S2O3制备SO2,另一产物为S;
(3)反应气体体积增多,△S>0;
(4)已知:①SO2+V2O5?SO3+V2O4 K1,
②$\frac{1}{2}$O2+V2O4?V2O5 K2,则-(①+②)×2可得2SO3(g)?2SO2(g)+O2(g),再得该反应的K;
(5))①由图可知,X越大,转化率越低;
②分解反应为吸热反应,温度高,转化率大;
(6)根据三段式列出平衡时各物质的量计算.
解答 解:(1)已知:①2H2SO4(l)═2SO2(g)+O2(g)+2H2O(g)△H=+550kJ•mol-1
②H2SO4(l)═SO3(g)+H2O(g)△H=+177kJ•mol-1
根据盖斯定律①-2×②可得:2SO3(g)=2SO2(g)+O2(g)△H=+196 kJ/mol;
故答案为:2SO3(g)=2SO2(g)+O2(g)△H=+196 kJ/mol;
(2)Na2S2O3溶液中滴加稀硫酸制备二氧化硫的方程为:S2O3 2-+2H+=S↓+SO2↑+H2O;
故答案为:S2O3 2-+2H+=S↓+SO2↑+H2O;
(3)反应气体体积增多,△S>0;
故答案为:>;
(4)已知::①SO2+V2O5?SO3+V2O4 K1,
$\frac{1}{2}$O2+V2O4?V2O5 K2,
则-(①+②)×2可得2SO3(g)?2SO2(g)+O2(g),K=$\frac{1}{{{K}_{1}}^{2}•{{K}_{2}}^{2}}$;
故答案为:$\frac{1}{{{K}_{1}}^{2}•{{K}_{2}}^{2}}$;
(5)①)①由图可知,X越大,转化率越低,升高温度转化率增大,则X表示压强;
故答案为:压强;
②由SO3(g)=SO2(g)+O2(g)△H>0,温度高,转化率大,图中等压强时L2对应的转化率大;
故答案为:L2>L1;
(6)在T℃时,物质的量为9mol、体积为2L的SO3(g)发生反应,SO3的平衡转化率25%,
2SO3(g)?2SO2(g)+O2(g),
起始量(mol):9 0 0
转化量(mol):2.25 2.25 1.125
平衡量(mol):6.75 2.25 1.125
维持体系总压p恒定,平衡时容器的体积为V,则$\frac{9}{6.75+2.25+1.125}=\frac{2L}{V}$,V=2.25L,则平衡常数K=$\frac{(2.25mol÷2.25L)^{2}×(1.125mol÷2.25L)}{(6.75mol÷2.25L)^{2}}$=$\frac{1}{18}$mol/L;
故答案为:$\frac{1}{18}$ mol/L.
点评 本题考查盖斯定律、氧化还原反应、及化学平衡等,为高频考点,把握发生的反应、平衡影响因素为解答的关键,侧重分析与应用能力的综合考查,题目难度中等.

| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | ||
| n(X) | n(Y) | n(Z) | n(Y) | ||
| ① | 600 | 1 | 0 | 0 | 0.8 |
| ② | 600 | 0.1 | a | 0.9 | 0.8 |
| ③ | 600 | 0 | 1.5 | 1.5 | b |
| ④ | 500 | 0.5 | 1.2 | 1.0 | c |
| A. | 实验②起始时V(逆)<v(正)且a=0.9 | |
| B. | 600℃时,该反应平衡常数K=3.2 moI/L | |
| C. | 实验③中b<1.2 | |
| D. | 若b>c,则△H<O |
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H
(1)已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g)△H1
C(石墨,s)+CO2(g)=2CO(g)△H2
则△H=△H1-3△H2(用含△H1、△H2代数式表示)
(2)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按表所示加入物质,反应经过一段时间后达到平衡.
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
②下列说法正确的是B(填字母).
A.若容器压强恒定,反应达到平衡状态
B.若容器内气体密度恒定,反应达到平衡状态
C.甲容器中CO的平衡转化率大于乙的
D.增加Fe2O3就能提高CO的转化率
II.利用空气催化氧化法制取联氨,其有关物质的转化如图1所示(R1、R2代表烃基).
①在图1示的转化中,化合价不变的一种元素是氢或H.
②反应中当有1mol NH3转化为N2H4时,保持溶液中酮的物质的量不变,需要消耗O2的物质的量为0.25mol.
③在温度一定和不补加溶液的条件下,缓慢通入NH3、O2混合气体,并充分搅拌.欲使生成的N2H4中不含NH3,可采取的措施有增大混合气体中氧气的含量.
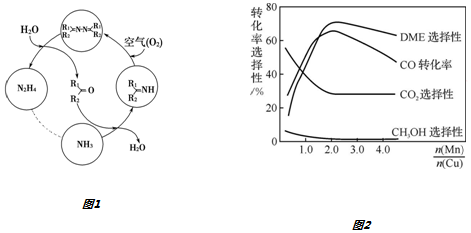
Ⅲ.采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(DME).观察如图2回答问题:催化剂中$\frac{n(Mn)}{n(Cu)}$约为2.0时最有利于二甲醚的合成.
| A. | 油脂是人体不可缺少的营养物质 | |
| B. | 油脂的水解产物是氨基酸 | |
| C. | 油脂主要在小肠中被消化吸收 | |
| D. | 脂肪中多不饱和酸含量越高,其营养价值也越高 |
| A. | 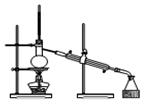 | B. | 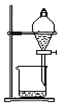 | C. |  | D. |  |
 请回答下列问题:
请回答下列问题: