题目内容
9.通过乙醇制取氢气通常有如下两条途径:a.CH3CH2OH(g)+H2O(g)=4H2(g)+2CO(g)△H1=+256.6kJ•mol-1
b.2CH3CH2OH(g)+O2(g)=6H2(g)+4CO(g)△H2=+27.6kJ•mol-1
则下列说法正确的是( )
| A. | 升高a的反应温度,乙醇的转化率增大 | |
| B. | 由b可知:乙醇的燃烧热为13.8kJ•mol-1 | |
| C. | 对反应b来说,增大O2浓度可使△H2的值增大 | |
| D. | 以上两种途径,制取等量的氢气,无论哪种途径,消耗的能量均相同. |
分析 A.为吸收反应,升高温度,平衡正向移动;
B.乙醇燃烧热中生成稳定氧化物为液态水、气态二氧化碳;
C.焓变与反应物的浓度无关;
C.制备等量的氢气时,a、b途径反应物不同,则起始物质的能量不同.
解答 解:A.为吸收反应,升高温度,平衡正向移动,则乙醇的转化率增大,故A正确;
B.乙醇燃烧热中生成稳定氧化物为液态水、气态二氧化碳,CO、氢气均不符合,则乙醇的燃烧热不是13.8kJ•mol-1,故B错误;
C.焓变与反应物的浓度无关,则对反应b来说,增大O2浓度而△H2的值不变,故C错误;
C.制备等量的氢气时,a、b途径反应物不同,则起始物质的能量不同,则以上两种途径,制取等量的氢气,消耗的能量不同,故D错误;
故选A.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、平衡移动、焓变为解答的关键,侧重分析与应用能力的考查,注意选项D为易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列贡献与中国科学家无关的是( )
| A. | 创立侯氏制碱法 | B. | 发现青蒿素 | ||
| C. | 合成结晶牛胰岛素 | D. | 发明元素周期表 |
17.根据下列实验现象所得出的结论错误的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 向KBrO2溶液中加入少量苯,然后通入少量Cl2 | 有机层呈橙色 | 氧化性:Cl2>KBrO2 |
| B | 向KNO3和KOH混合溶液中加入铝粉并加热,将湿润的红色石蕊试纸放在试管口 | 试纸变为蓝色 | NO${\;}_{3}^{-}$被还原为NH3 |
| C | 向0.1mol•L-1的Na2CO3溶液中加入两滴酚酞,溶液显浅红色,微热 | 红色加深 | 盐类水解是吸热反应 |
| D | 将0.1mol•L-1的MgSO4溶液滴入到NaOH溶液中至不再有沉淀产生,再滴加0.1mol•L-1的CuSO4溶液 | 白色沉淀逐渐变为蓝色沉淀 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| A. | A | B. | B | C. | C | D. | D |
14.下列有机物的同分异构体数目最多的( )
| A. | C5H12 | B. | 甲苯的二氯代物 | C. | C6H14 | D. | C5H12O(醇类结构) |
16.在含Ba2+、Ca2+、Ag+的酸性溶液中,可能存在的阴离子是( )
| A. | NO3- | B. | Cl- | C. | CO32- | D. | SO32- |
17.下列有机物命名正确的是( )
| A. | 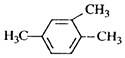 1,3,4-三甲苯 1,3,4-三甲苯 | B. | CH3CH(Cl)CH3 2-氯丙烷 | ||
| C. | 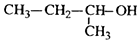 2-甲基-1-丙醇 2-甲基-1-丙醇 | D. | 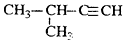 2-甲基-3-丁炔 2-甲基-3-丁炔 |

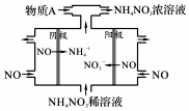 NO2是形成雾霾天气的原因之一.
NO2是形成雾霾天气的原因之一. .
.