题目内容
13.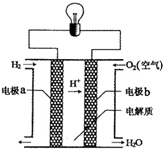 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )| A. | 该电池工作时电能转化为化学能 | |
| B. | 该电池中电极b是负极 | |
| C. | 外电路中电子由电极b通过导线流向电极a | |
| D. | 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
分析 A.该装置能自发的进行氧化还原反应,属于原电池;
B.燃料电池中,通入燃料的电极为负极;
C.电子从负极沿导线流向正极;
D.燃料电池的正负极气体无需在电池内部储存.
解答 解:A.该装置能自发的进行氧化还原反应,属于原电池,是将化学能转化为电能的装置,故A错误;
B.燃料电池中,通入燃料的电极为负极,所以a是负极,故B错误;
C.电子从负极沿导线流向正极,a是负极、b是正极,则电子由电极a通过导线流向电极b,故C错误;
D.氢氧燃料电池不需要将正极和负极反应物全部储藏在电池内,故D正确;
故选D.
点评 本题考查了原电池原理,根据原电池概念、燃料电池中得失电子、电子流向等知识点来分析解答即可,题目难度不大

练习册系列答案
相关题目
1.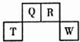 短周期元素Q、R、T、W在周期表中的位置如图所示,其中,T所处周期序数与主族序数相等,则下列说法正确的是( )
短周期元素Q、R、T、W在周期表中的位置如图所示,其中,T所处周期序数与主族序数相等,则下列说法正确的是( )
 短周期元素Q、R、T、W在周期表中的位置如图所示,其中,T所处周期序数与主族序数相等,则下列说法正确的是( )
短周期元素Q、R、T、W在周期表中的位置如图所示,其中,T所处周期序数与主族序数相等,则下列说法正确的是( )| A. | 元素T和W各自形成的简单离子都能促进水的电离 | |
| B. | 元素Q的含氧酸一定是二元弱酸 | |
| C. | 简单离子半径:W>T>R | |
| D. | 常温下,T的单质能溶于R的最高价氧化物的水化物的浓溶液中 |
8.下列关于电解质溶液的叙述正确的是( )
| A. | 常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为c(Cl-)>c(NH+4)>c(H+)>c(OH-) | |
| B. | 将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | |
| C. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 | |
| D. | 将pH=4的醋酸溶液和pH=10的氢氧化钠溶液等体积混合,所得溶液的pH一定大于7 |
18.下列有机物分子中可形成顺反异构的是( )
| A. | CH3CH=CHBr | B. | CH3-Cl | C. | CH3CH=CH2 | D. | CH3CH=C(CH3)2 |
2.下列说法不正确的是( )
| A. | 室温下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷 | |
| B. | 乙二酸俗称草酸,具有还原性,可以使酸性高锰酸钾溶液褪色 | |
| C. | 银氨溶液和氢氧化铜悬浊液可以较长时间存放 | |
| D. | 油脂在酸性或碱性条件下均可发生水解反应,且产物不相同 |
3.下列反应属于不属于取代反应的是( )
| A. | 油脂的水解 | |
| B. | 在一定条件下,苯与浓硝酸反应制取硝基苯 | |
| C. | 乙醛与氢气的反应 | |
| D. | 甲烷与氯气在光照条件下反应 |
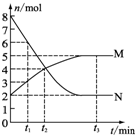 一定温度下,在容积为V L的密闭容器中进行aN(g)?bM(g)的放热反应,M、N物质的量随时间的变化曲线如图所示:
一定温度下,在容积为V L的密闭容器中进行aN(g)?bM(g)的放热反应,M、N物质的量随时间的变化曲线如图所示: