题目内容
下列溶液Cl-物质的量浓度与50mL 1mol?L-1AlCl3溶液中Cl-物质的量浓度相等的是( )
| A、150 mL 1 mol?L-1NaCl溶液 |
| B、75 mL 1.5 mol?L-1CaCl2溶液 |
| C、150 mL 3 mol?L-1KClO3溶液 |
| D、50 mL 3 mol?L-1MgCl2溶液 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:50mL 1mol?L-1 AlCl3溶液中Cl-物质的量浓度是3mol/L,以此解答即可.
解答:
解:A.150mL 1mol?L-1氯化钠溶液中c(Cl-)=1 mol?L-1×1=1mol/L,故A错误;
B.75mL 1.5mol?L-1氯化钙溶液中c(Cl-)=1.5mol?L-1×2=3mol/L,故B正确;
C.100ml 3mol?L-1KClO3溶液中不含有Cl-,故C错误;
D.50mL 3mol?L-1氯化镁溶液中c(Cl-)=3mol?L-1×2=6mol/L,故D错误.
故选B.
B.75mL 1.5mol?L-1氯化钙溶液中c(Cl-)=1.5mol?L-1×2=3mol/L,故B正确;
C.100ml 3mol?L-1KClO3溶液中不含有Cl-,故C错误;
D.50mL 3mol?L-1氯化镁溶液中c(Cl-)=3mol?L-1×2=6mol/L,故D错误.
故选B.
点评:本题考查物质的量浓度的计算,为高频考点,侧重于学生的计算能力的考查,题目难度不大,本题注意把握有关公式的运用.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
某溶液中加入铝粉能产生氢气,则该溶液中肯定不能大量共存的离子组是( )
| A、AlO2-、NO3-、CO32-、Na+ |
| B、Na+、Al3+、H+、Cl- |
| C、NO3-、NH4+、K+、Cl- |
| D、NO3-、K+、AlO2-、OH- |
20℃时某盐的溶解度为25g.现有10%的该盐溶液Mg,要使它成为20℃时的饱和溶液,可采用的方法是( )
A、蒸发掉溶剂的
| ||
B、蒸发掉
| ||
C、加入
| ||
D、加入
|
下列关于化学用语的表示错误的是( )
A、Na+的电子排布图: |
B、氯离子的结构示意图 |
C、甲基的电子式: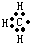 |
| D、硫离子的核外电子排布式:1s22s22p63s23p6 |
下列说法正确的是( )
| A、摩尔表示物质的质量的单位 |
| B、10gHF含有0.5molHF分子 |
| C、2gH2的体积约为22.4L |
| D、物质的摩尔质量等于其相对原子质量或相对分子质量 |
下列离子方程式正确的是( )
| A、H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、苯酚与通入少量的CO2的反应:2C6H5O-+CO2+H2O→2 C6H5OH+Na2CO3 |
| C、AlCl3溶液中加入过量的浓氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| D、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
下列离子方程式书写正确的是( )
| A、硫酸铜溶液中滴加氢氧化钡溶液Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓ |
| B、稀盐酸和碳酸钙反应 CO32-+2H+=CO2↑+H2O |
| C、明矾溶于水产生Al(OH)3胶体:Al3++3H2O═Al(OH)3↓+3H+ |
| D、铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
元素X、Y、Z原子序数之和为36,Y、Z在同一周期,X,Z在同一主族,X原子最外层电子数是Y原子最外层电子数的3倍.下列说法正确的是( )
| A、同主族元素中Y的气态氢化物最稳定 |
| B、Z的最高价氧化物对应的水化物不稳定 |
| C、X与Y可形成共价化合物 |
| D、X与Z所形成的化合物属于酸性氧化物 |