题目内容
 一定条件下发生反应:
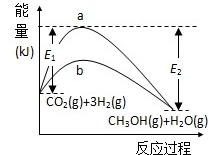
一定条件下发生反应:能量(kJ)反应过程CH3OH(g)+H2O(g)CO2(g)+3H2(g)baE2E1
CO2(g)+3H2(g)CH3OH(g)+H2O(g),如图表示该反应进行过程中的能量变化.
(1)图中曲线
A.提高反应速率
B.提高CO2的转化率
C.降低反应活化能
D.改变反应的△H
(2)CO2(g)+3H2(g)CH3OH(g)+H2O(g)的化学平衡常数的表达式K=
(3)用含E1、E2的表达式表示
CO2(g)+3H2(g)CH3OH(g)+H2O(g)的△H=
(4)一定温度下,在体积为2L的容积固定的密闭容器中,充入2molCO2、6molH2,经10min反应达到平衡状态W,生成1molCH3OH.CO2的转化率为
考点:化学平衡的计算,化学平衡的影响因素
专题:化学平衡专题
分析:(1)加催化剂降低反应所需的活化能;催化剂对平衡无影响;
(2)根据CO2(g)+3H2(g)=CH3OH(g)+H2O(g)结合平衡常数的含义书写;由于可知该反应为放热反应,升高温度平衡逆移;
(3)△H=正反应的活化能-逆反应的活化能;
(4)根据已知数据利用三段式计算出各物质的反应的量和平衡是的物质的量,根据转化率的公式计算,由v(H2)=
计算;从逆反应开始建立化学平衡,且各组分的平衡浓度与平衡状态W完全相同,则把生成物完全转化为反应物与原来的初始浓度相同即可.
(2)根据CO2(g)+3H2(g)=CH3OH(g)+H2O(g)结合平衡常数的含义书写;由于可知该反应为放热反应,升高温度平衡逆移;
(3)△H=正反应的活化能-逆反应的活化能;
(4)根据已知数据利用三段式计算出各物质的反应的量和平衡是的物质的量,根据转化率的公式计算,由v(H2)=
| ||
| t |
解答:
解:(1)加催化剂降低反应所需的活化能,所以b曲线表示使用催化剂时的反应进程;
A.加催化剂降低反应所需的活化能,能提高反应速率,故A正确;
B.加催化剂,化学平衡不移动,则CO2的转化率不变,故B错误;
C.加催化剂降低反应所需的活化能,故C正确;
D.加催化剂,对反应物与生成物总能量相对大小无影响,即对△H无影响,故D错误;
故答案为:b;AC;
(2)已知CO2(g)+3H2(g)=CH3OH(g)+H2O(g),则平衡常数K=
;由于可知该反应反应物的总能量大于生成物的总能量,为放热反应,升高温度平衡逆移,则K减小;
故答案为:
;减小;
(3)△H=正反应的活化能-逆反应的活化能,则△H=E1-E2,
故答案为:E1-E2;
(4)CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
开始:2mol 6mol 0 0
转化:1mol 3mol 1mol 1mol
平衡:1mol 3mol 1mol 1mol
则CO2的转化率为
×100%=50%;
H2的浓度变化表示的平均反应速率v(H2)=
=0.15 mol?L-1?min-1;
该温度下,在体积为1L的容积固定的密闭容器中,从逆反应开始建立化学平衡,且各组分的平衡浓度与平衡状态W完全相同,则把生成物完全转化为反应物与原来的初始浓度相同即可,原来反应物的初始浓度为c(CO2)=
=
=1mol/L,c(H2)=
=
=3mol/L,若完全反应转化为生成物,则生成物的浓度分别为1mol/L、1mol/L,当体积为1L时,则物质的量为n(CH3OH)=1mol,n(H2O)=1mol,所以在体积为1L的容积固定的密闭容器中,起始时充入容器物质的量为n(CH3OH)=1mol,n(H2O)=1mol时,达到平衡时与原平衡相同;
故答案为:50%;0.15 mol?L-1?min-1;1 mol;1 mol.
A.加催化剂降低反应所需的活化能,能提高反应速率,故A正确;
B.加催化剂,化学平衡不移动,则CO2的转化率不变,故B错误;
C.加催化剂降低反应所需的活化能,故C正确;
D.加催化剂,对反应物与生成物总能量相对大小无影响,即对△H无影响,故D错误;
故答案为:b;AC;
(2)已知CO2(g)+3H2(g)=CH3OH(g)+H2O(g),则平衡常数K=
| c(CH3OH)?c(H2O) |
| c(CO2)?c3(H2) |
故答案为:
| c(CH3OH)?c(H2O) |
| c(CO2)?c3(H2) |
(3)△H=正反应的活化能-逆反应的活化能,则△H=E1-E2,
故答案为:E1-E2;
(4)CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
开始:2mol 6mol 0 0
转化:1mol 3mol 1mol 1mol
平衡:1mol 3mol 1mol 1mol
则CO2的转化率为
| 1mol |
| 2mol |
H2的浓度变化表示的平均反应速率v(H2)=
| ||
| 10min |
该温度下,在体积为1L的容积固定的密闭容器中,从逆反应开始建立化学平衡,且各组分的平衡浓度与平衡状态W完全相同,则把生成物完全转化为反应物与原来的初始浓度相同即可,原来反应物的初始浓度为c(CO2)=
| n |
| V |
| 2mol |
| 2L |
| n |
| V |
| 6mol |
| 2L |
故答案为:50%;0.15 mol?L-1?min-1;1 mol;1 mol.
点评:本题涉及反应速率和化学平衡的综合应用,注意把握催化剂对反应热和活化能的影响,培养学生的平衡思想,题目综合性强,难度中等,三段式是解平衡题常用的方法.

练习册系列答案
相关题目
下图所示实验操作中,正确的是( )
A、 检查容量瓶是否漏水 |
B、 给液体加热 |
C、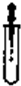 滴加液体 |
D、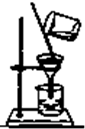 过滤 |
用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是( )
| A、未用标准液润洗碱式滴定管 |
| B、滴定终点读数时,俯视滴定管的刻度,其它操作均正确 |
| C、盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗 |
| D、滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 |
下列气体不能用浓H2SO4干燥的是( )
| A、CO2 |
| B、SO2 |
| C、NH3 |
| D、HC1 |
下列分子是非极性分子的是( )
| A、H2O |
| B、NH3 |
| C、O2 |
| D、CO2 |
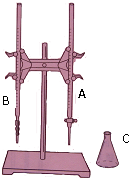 某同学利用如图装置,用0.1000mol/L的氢氧化钾溶液测定某未知浓度的盐酸溶液的物质的量浓度,其操作可分解为如下几步:
某同学利用如图装置,用0.1000mol/L的氢氧化钾溶液测定某未知浓度的盐酸溶液的物质的量浓度,其操作可分解为如下几步: