题目内容
铜和稀硝酸反应的化学方程式为:3Cu+8HNO3 3Cu(NO3)2+2NO↑+4H2O,其中铜元素的化合价________(填“升高”或“降低”),氮元素被________(填“氧化”或“还原”,下同),稀硝酸的作用是________、________.在该反应中,若消耗了32g铜,则转移电子数目为________mol.
3Cu(NO3)2+2NO↑+4H2O,其中铜元素的化合价________(填“升高”或“降低”),氮元素被________(填“氧化”或“还原”,下同),稀硝酸的作用是________、________.在该反应中,若消耗了32g铜,则转移电子数目为________mol.
升高 还原 酸 氧化剂 1
分析:元素化合价变化是氧化还原反应的特征,元素化合价升高的是还原剂,失电子被氧化,发生氧化反应;元素化合价降低的做氧化剂得到电子,发生还原反应;依据反应产物和元素化合价变化分析物质的作用,根据氧化还原反应电子守恒计算转移电子数.
解答:铜和稀硝酸反应的化学方程式为:3Cu+8HNO3 3Cu(NO3)2+2NO↑+4H2O,其中铜元素的化合价升高;氮元素化合价从+5价变化为+2价,化合价降低做氧化剂被还原发生还原反应;硝酸在反应前后生成一氧化氮气体的做氧化剂,生成硝酸铜的硝酸化合价未变化,做酸; 反应中若消耗了32g铜物质的量为0.5mol,则转移电子数目为1mol,
3Cu(NO3)2+2NO↑+4H2O,其中铜元素的化合价升高;氮元素化合价从+5价变化为+2价,化合价降低做氧化剂被还原发生还原反应;硝酸在反应前后生成一氧化氮气体的做氧化剂,生成硝酸铜的硝酸化合价未变化,做酸; 反应中若消耗了32g铜物质的量为0.5mol,则转移电子数目为1mol,
故答案为:升高;还原;酸;氧化剂;1.
点评:本题考查了氧化还原反应的基础知识,掌握概念,理解含义,标注元素化合价变化是解题关键,题目较简单.
分析:元素化合价变化是氧化还原反应的特征,元素化合价升高的是还原剂,失电子被氧化,发生氧化反应;元素化合价降低的做氧化剂得到电子,发生还原反应;依据反应产物和元素化合价变化分析物质的作用,根据氧化还原反应电子守恒计算转移电子数.
解答:铜和稀硝酸反应的化学方程式为:3Cu+8HNO3
 3Cu(NO3)2+2NO↑+4H2O,其中铜元素的化合价升高;氮元素化合价从+5价变化为+2价,化合价降低做氧化剂被还原发生还原反应;硝酸在反应前后生成一氧化氮气体的做氧化剂,生成硝酸铜的硝酸化合价未变化,做酸; 反应中若消耗了32g铜物质的量为0.5mol,则转移电子数目为1mol,
3Cu(NO3)2+2NO↑+4H2O,其中铜元素的化合价升高;氮元素化合价从+5价变化为+2价,化合价降低做氧化剂被还原发生还原反应;硝酸在反应前后生成一氧化氮气体的做氧化剂,生成硝酸铜的硝酸化合价未变化,做酸; 反应中若消耗了32g铜物质的量为0.5mol,则转移电子数目为1mol,故答案为:升高;还原;酸;氧化剂;1.
点评:本题考查了氧化还原反应的基础知识,掌握概念,理解含义,标注元素化合价变化是解题关键,题目较简单.

练习册系列答案
相关题目
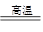 Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化
Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化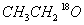 在一定条件下生成酯的化学方程式(标明
在一定条件下生成酯的化学方程式(标明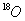 的位置) 。
的位置) 。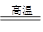 Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化
Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化