题目内容
13.若NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 0.1 L l mol•L-1 Na2CO3溶液中,阴离子总数大于0.1NA | |
| B. | 标准状况下,22.4 L氦气中含有的原子数为2NA | |
| C. | 100 g 98%的浓硫酸中,氧原子总数为4NA | |
| D. | 4.6 g组成为C2H6O的有机物,C-H键数目不一定为0.5NA |
分析 A、碳酸根水解会导致阴离子个数增多;
B、求出氦气的物质的量,然后根据氦气为单原子分子来分析;
C、在浓硫酸溶液中,除了浓硫酸外,水也含氧原子;
D、C2H6O可能为乙醇,还可能为二甲醚.
解答 解:A、碳酸根水解会导致阴离子个数增多,故溶液中的阴离子的个数多于0.1NA个,故A正确;
B、标况下22.4L氦气的物质的量为1mol,而氦气为单原子分子,故1mol氦气中含NA个原子,故B错误;
C、在浓硫酸溶液中,除了浓硫酸外,水也含氧原子,故溶液中的氧原子的个数多于4NA个,故C错误;
D、C2H6O可能为乙醇,还可能为二甲醚,当为乙醇时,4.6g此有机物中含0.5NA个C-H键,但当为二甲醚时,含0.6NA条,故D正确.
故选AD.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列说法正确的是( )(NA表示阿伏加德罗常数的值)
| A. | 1mol石炭酸根含有的电子数目为49NA | |
| B. | 标况下1L已烷完全燃烧后恢复至原状态,生成气态物质分子数为6 NA22.4 | |
| C. | 1mol甲基含有9NA个电子 | |
| D. | 0.1mol甘油与足量的钠反应,可生成氢气3.36L |
8.通常人们把拆开 1mol 某化学键吸收的能量看成该化学键的键能.键能的大小可以衡量化 学键的强弱,也可以估计化学反应的反应热.下列是一些化学键的键能.
根据键能数据估算反应 CH4+4F2=CF4+4HF 每消耗 1mol CH4的热效应( )
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | 放热 1940 kJ | B. | 吸热 1940 kJ | C. | 放热 485 kJ | D. | 吸热 485 kJ |
18.分类方法对化学学科的发展起到了非常重要的作用.下列分类标准合理的是( )
①根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等
②氧化物不是酸性氧化物就是碱性氧化物
③根据是否含有氧原子,酸可分为含氧酸和无氧酸.
①根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等
②氧化物不是酸性氧化物就是碱性氧化物
③根据是否含有氧原子,酸可分为含氧酸和无氧酸.
| A. | 仅①③ | B. | 仅②③ | C. | 仅①② | D. | 仅③ |
5.下列说法正确的是( )
| A. | 金属钠投入氯化亚铁溶液可制取氢氧化铁胶体 | |
| B. | 镁带燃烧可以用二氧化碳灭火器扑灭 | |
| C. | 铁能从硫酸铜溶液中置换出铜,生成硫酸铁 | |
| D. | 硅酸的酸酐是二氧化硅,能溶于氢氟酸 |
2.常温下,下列各组离子在指定的条件下一定能大量共存的是( )
| A. | 加铝粉能产生大量H2的溶液中:Na+、NH4+、NO3-、Cl- | |
| B. | 使甲基橙变红色的溶液中:K+、NH4+、HCO3-、Cl- | |
| C. | 由c(H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO3- | |
| D. | 水电离出的c(H+)=10-12mol•L-1的溶液中:Mg2+、Cu2+、SO42-、K+ |
3.将铁屑溶于过量盐酸后,再加入或通入下列物质,会有Fe3+生成的是( )
| A. | 硫酸 | B. | 二氧化碳 | C. | 硝酸锌 | D. | 氯化铜 |
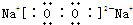 ,其中含有的化学键类型为离子键、非极性键
,其中含有的化学键类型为离子键、非极性键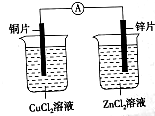 某实验小组拟用铜片、锌片、CuCl2溶液、ZnCl2溶液等设计原电池.并将装置图画到了如图所示程度.
某实验小组拟用铜片、锌片、CuCl2溶液、ZnCl2溶液等设计原电池.并将装置图画到了如图所示程度.