题目内容
1.下列有关非金属元素说法正确的是( )| A. | 二氧化氯具有还原性,可用于自来水的杀菌消毒 | |
| B. | SO2具有氧化性,可用于漂白纸浆 | |
| C. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| D. | 硅是重要的半导体材料,常用于制作光导纤维 |
分析 A.二氧化氯具有强的氧化性;
B.二氧化硫能够漂白纸浆是因为其具有漂白性;
C.依据液氨汽化时要吸收大量的热,具有制冷作用解答;
D.二氧化硅为光导纤维主要原料.
解答 解:A.二氧化氯具有氧化性,可用于自来水的杀菌消毒,故A错误;
B.二氧化硫能够漂白纸浆是因为其具有漂白性,与二氧化硫的氧化性无关,故B错误;
C.液氨汽化时要吸收大量的热,具有制冷作用,可用作制冷剂,故C正确;
D.二氧化硅为光导纤维主要原料,故D错误;
故选:C.
点评 本题考查了元素化合物知识,涉及二氧化硫、液氨、硅、二氧化硅性质和用途,熟悉相关物质的性质是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列涉及无机化合物的分离提纯,其中说法正确的是( )
| A. | 除去CO2中混有的少量SO2,可将气体通过酸性高锰酸钾溶液 | |
| B. | 除去SiO2中混有的少量Al2O3,可以用NaOH溶液洗涤 | |
| C. | 除去Fe粉中的少量Mg粉,可以将该粉末用稀硝酸洗涤,然后过滤 | |
| D. | 除去NO2气体中混有的少量NO气体,可以向该气体中充入过量空气 |
12.根据下列反应进行判断,下列各微粒氧化能力由强到弱的顺序正确的是( )
①ClO3-+5Cl-+6H+═3Cl2+3H2O
②2FeCl3+2KI═2FeCl2+2KCl+I2
③2FeCl2+Cl2═2FeCl3.
①ClO3-+5Cl-+6H+═3Cl2+3H2O
②2FeCl3+2KI═2FeCl2+2KCl+I2
③2FeCl2+Cl2═2FeCl3.
| A. | ClO3->Cl2>I2>Fe3+ | B. | Cl2>ClO3->I2>Fe3+ | ||
| C. | ClO3->Cl2>Fe3+>I2 | D. | ClO3->Fe3+>Cl2>I2 |
9.下列说法正确的是( )
| A. | 红宝石、珍珠、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐 | |
| B. | 石油裂解、煤的气化、海水制镁、纤维素制火棉等过程中都包含化学变化 | |
| C. | 氢氧燃料电池、丹尼尔电池、硅太阳能电池中都利用了原电池原理 | |
| D. | 纤维素、PLA、纤维二糖、甲壳素、硝化纤维等都是高分子化合物 |
13.下列鉴别方法可行的是( )
①用NaOH溶液鉴别Al3+、Mg2+、Cu2+
②用Ba(NO3)2溶液鉴别Cl-、SO42-、和CO32-
③用KMnO4酸性溶液鉴别HCHO、CH2=CH2和CO2
④用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷.
①用NaOH溶液鉴别Al3+、Mg2+、Cu2+
②用Ba(NO3)2溶液鉴别Cl-、SO42-、和CO32-
③用KMnO4酸性溶液鉴别HCHO、CH2=CH2和CO2
④用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷.
| A. | ①② | B. | ①④ | C. | ②③ | D. | ②④ |
10.下列有关物质性质或应用的说法正确的是( )
| A. | 二氧化锰具有强氧化性,能将双氧水氧化为氧气 | |
| B. | 硅为半导体,常用作光导纤维 | |
| C. | 炭具有强还原性,高温下能将二氧化硅还原为硅 | |
| D. | 二氧化硫具有漂白性,与氯水混合使用效果会更好 |
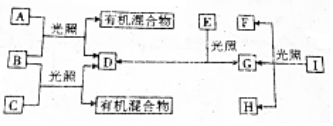
 如图所示:淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应.A、B、C都可以被强还原剂还原成为D(C6H14O6).已知,相关物质被氧化的难易次序是:RCHO最易,R-CH2OH次之
如图所示:淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应.A、B、C都可以被强还原剂还原成为D(C6H14O6).已知,相关物质被氧化的难易次序是:RCHO最易,R-CH2OH次之  最难.
最难.
 ,有机物C的结构简式为
,有机物C的结构简式为 ,其苯环上的二氯代物共有6种.
,其苯环上的二氯代物共有6种.