题目内容
下表是元素周期表的一部分,按要求填空:
(1)写出元素符号:A B D ;
(2)A-和B+的电子层结构 (相同或不相同),都与 原子(填元素符号)电子层结构相同;
(3)能生成两性氢氧化物的元素是 (填写元素符号),其最高价氧化物对应水化物与强酸、强碱溶液反应的离子方程式分别是 , .
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | A | |||||||
| 3 | B | C | D |
(2)A-和B+的电子层结构
(3)能生成两性氢氧化物的元素是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:(1)由元素在周期中位置,可知A为F、B为Na、C为Al、D为Ar;
(2)F-和Na+的核外电子数都是10,电子层结构,与Ne原子的电子层结构相同;
(3)氢氧化铝是两性氢氧化物;氢氧化铝与强酸反应生成铝盐与水,与强碱反应生成偏铝酸盐与水.
(2)F-和Na+的核外电子数都是10,电子层结构,与Ne原子的电子层结构相同;
(3)氢氧化铝是两性氢氧化物;氢氧化铝与强酸反应生成铝盐与水,与强碱反应生成偏铝酸盐与水.
解答:
解:(1)由元素在周期中位置,可知A为F、B为Na、C为Al、D为Ar,故答案为:F;Na;Ar;
(2)F-和Na+的核外电子数都是10,电子层结构,与Ne原子的电子层结构相同,故答案为:相同;Ne;
(3)Al元素的氢氧化物--氢氧化铝,属于两性氢氧化物;氢氧化铝与强酸反应生成铝盐与水,反应离子方程式为:Al(OH)3 +3H+═Al3++3H2O,与强碱反应生成偏铝酸盐与水,反应离子方程式为:Al(OH)3 +OH-═AlO2-+2H2O,
故答案为:Al;Al(OH)3 +3H+═Al3++3H2O;Al(OH)3 +OH-═AlO2-+2H2O.
(2)F-和Na+的核外电子数都是10,电子层结构,与Ne原子的电子层结构相同,故答案为:相同;Ne;
(3)Al元素的氢氧化物--氢氧化铝,属于两性氢氧化物;氢氧化铝与强酸反应生成铝盐与水,反应离子方程式为:Al(OH)3 +3H+═Al3++3H2O,与强碱反应生成偏铝酸盐与水,反应离子方程式为:Al(OH)3 +OH-═AlO2-+2H2O,
故答案为:Al;Al(OH)3 +3H+═Al3++3H2O;Al(OH)3 +OH-═AlO2-+2H2O.
点评:本题考查元素周期表、原子结构、常用化学用语等,比较基础,整体把握元素周期表的晶体,注意对基础知识的理解掌握.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
常温下,某溶液中由水电离产生的c(H+)等于10-11mol?L-1,则该溶液的pH可能是( )
| A、3 | B、7 | C、8 | D、12 |
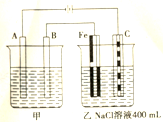 下图为相互串联的甲乙两个电解池,试回答:
下图为相互串联的甲乙两个电解池,试回答: