题目内容
13.用一种试剂就能鉴别出NaN03、BaCl2、Na2SO3、Ba(HCO3)2四种溶液.该试剂是稀硫酸,相关反应的离子方程式为SO42-+Ba2+=BaSO4↓,2H++SO32-=H2O+SO2↑,2H++SO42-+Ba2++2HCO3-=BaSO4↓+2H2O+2CO2↑.分析 检验BaCl2,需要通过生成沉淀的方法;检验Na2SO3,可通过生成二氧化硫气体的方法;检验Ba(HCO3)2,既可以生成沉淀,也可以生成二氧化碳气体,综合以上分析,可用稀硫酸检验,分别写出反应的离子方程式.
解答 解:检验BaCl2时可通过生成硫酸钡沉淀的方法;
检验Na2SO3可通过与酸反应生成二氧化硫气体的方法;
检验Ba(HCO3)2,既可以生成硫酸钡沉淀,同时可生成二氧化碳气体,
根据以上分析可知,用一种试剂检验四种溶液,可用稀H2SO4溶液,
稀硫酸BaCl2、Na2SO3、Ba(HCO3)2的离子反应分别为:SO42-+Ba2+=BaSO4↓、2H++SO32-=H2O+SO2↑、2H++SO42-+Ba2++2HCO3-=BaSO4↓+2H2O+2CO2↑,
故答案为:稀硫酸;SO42-+Ba2+=BaSO4↓、2H++SO32-=H2O+SO2↑、2H++SO42-+Ba2++2HCO3-=BaSO4↓+2H2O+2CO2↑.
点评 本题考查了物质的检验和鉴别方法、离子方程式书写,题目难度中等,明确常见物质检验方案的设计方法为解答关键,注意掌握离子方程式的书写原则,试题培养了学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.设阿伏加德罗常数的值为NA,下列说法正确的是( )
| A. | 常温常压下,18g H2O中含有的原子总数为3NA | |
| B. | 在标准状况下,22.4L苯的物质的量为1mol | |
| C. | 1mol/L NaOH溶液中含有的Na+数为NA | |
| D. | 22gCO2与标准状况下11.2LHCI所含的分子数不相同 |
4.等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)?2Z(g),△H<0,下列叙述正确的是( )
| A. | 平衡常数K值越大,X的转化率越大 | |
| B. | 达到平衡时,反应速率:v正(X)=2v逆(Z) | |
| C. | 达到平衡后,降低温度,正反应速率减小的倍数小于逆反应减小的倍数 | |
| D. | 达到平衡后,升高温度或增大压强都有利于该平衡向逆反应方向移动 |
19.下列离子方程式错误的是( )
| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO${\;}_{4}^{2-}$═BaSO4↓+2H2O | |
| B. | 酸性介质中KMnO4氧化H2O2:2MnO${\;}_{4}^{-}$+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | 0.01mol•L-1NH4Al(SO4)2溶液与0.02mol•L-1Ba(OH)2溶液等体积混合:NH${\;}_{4}^{+}$+Al5++SO${\;}_{4}^{2-}$+Ba2++4OH-═BaSO4↓+Al(OH)5↓+NH5•H2O | |
| D. | 铅蓄电池充电时的正极反应:PbSO4+2H2O-2e-═PbO2+4H++SO${\;}_{4}^{2-}$ |
20. 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应开始到10s时,用Z表示的反应速率为0.158 mol•(L•s)-1 | |
| B. | 反应开始到10s时,X的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应的化学方程式为X(g)+Y(g)?2Z(g) | |
| D. | 反应开始到10 s时,Y的转化率为39.5% |
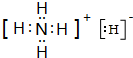 该物质能与水剧烈反应生成两种气体,两种气体的化学式分别是NH3、H2
该物质能与水剧烈反应生成两种气体,两种气体的化学式分别是NH3、H2